5

| CBDCA | カルボプラチン | |
| CDDP | シスプラチン | |
| CPT-11 | イリノテカン | |
| DTX | ドセタキセル | |
| GEM | ゲムシタビン | |
| nab-PTX | ナブパクリタキセル | |
| PEM | ペメトレキセド | |
| PTX | パクリタキセル | |
| VNR | ビノレルビン | |
| プラチナ製剤 | CDDPとCBDCAの総称 | |
| EGFR-TKI | ゲフィチニブ・エルロチニブ・アファチニブの総称 | |
| ALK | anaplastic lymphoma kinase | 未分化リンパ腫キナーゼ |
| ECOG | eastern cooperative oncology group | 米国東海岸癌臨床試験グループ |
| EGFR | epidermal growth factor receptor | 上皮成長因子受容体 |
| ORR | objective response rate | 客観的奏効率 |
| OS | overall survival | 全生存期間 |
| PFS | progression free survival | 無増悪生存期間 |
| PS | performance status | 一般状態 |
| QOL | quality of life | 生活の質 |
| TKI | tyrosine kinase inhibitor | チロシンキナーゼ阻害剤 |
ECOG(Eastern Cooperative Oncology Group) Performance Status
| PS | |
|---|---|
| 0 | 無症状で社会活動ができ,制限を受けることなく発病前と同等に振る舞える。 |
| 1 | 軽度の症状があり,肉体労働は制限を受けるが,歩行,軽労働や座業はできる。例えば軽い家事,事務など |
| 2 | 歩行や身の回りのことはできるが,時に少し介助がいることもある。軽労働はできないが,日中の50%以上は起居している。 |
| 3 | 身の回りのある程度のことはできるが,しばしば介助がいり,日中の50%以上は就床している。 |
| 4 | 身の回りのこともできず,常に介助がいり,終日就床を必要としている。 |
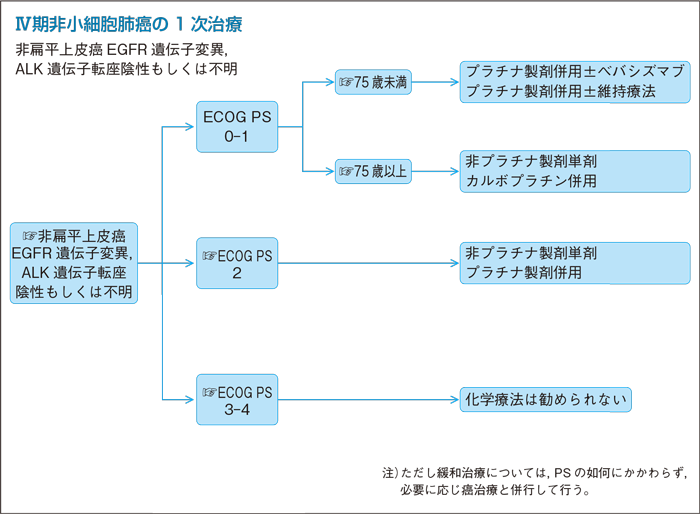
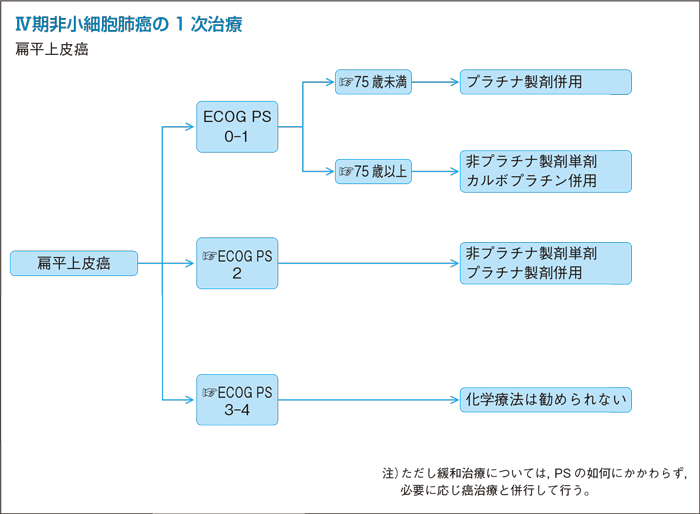
補足:高齢者の定義
しかしながら,日本の臨床試験においては75歳以上の患者が除外されていることが多く,75歳以上の高齢者のデータは少ない。また,近年の70歳以上の高齢者を対象とした第3世代抗癌剤単剤とプラチナ製剤併用療法を比較した2編の第Ⅲ相試験において両試験とも登録された患者の多くが75歳以上であった。
以上より,本ガイドラインでは「75歳以上」を高齢者と定義する。
補足:維持療法(Maintenance)の定義
- Switch maintenance:プラチナ併用化学療法による導入療法後,導入療法で使用した薬剤とは別の薬剤に切り替えて投与する方法。
- Continuation maintenance:プラチナ併用化学療法による導入療法後,プラチナ製剤と併用した薬剤を継続して投与する方法。
- 推 奨
- ECOG PS 0-2で全身状態良好なⅣ期非小細胞肺癌患者に対する化学療法は生存期間を延長し,QOLも改善することから,行うよう勧められる。(グレードA)
メタアナリシスによって化学療法が緩和治療に対して有意に生存に寄与していることが示されている1)。これは1年生存率にして9%(20%から29%)の改善,もしくは約1.5カ月のOS延長に値する。また,第3世代抗癌剤を用いたレジメンの検討では,第3世代単剤治療でも緩和治療に比して1年生存率で約7%の改善を示していることを示した2)。
一方で重大な毒性については,別のメタアナリシスで進行非小細胞肺癌における化学療法の治療関連死が1.26%であったと報告されており,その内訳は発熱性好中球減少,虚血や血栓などの心血管系の毒性,肺炎や間質性肺障害などの肺毒性であった3)。
QOLに関しては,第3世代抗癌剤単剤と緩和治療との比較において前者でのQOL改善が報告されている4)。また,GEMとCBDCA+GEMの第Ⅲ相試験では,後者がOS・PFS延長を示すと同時にQOLは同等であったとされた5)。ゲフィチニブ単剤はEGFR遺伝子変異陽性患者を対象としたCBDCA+PTXとの第Ⅲ相試験においてQOL指標の一部が有意に優れていたことが示されている6)。
以上より,ECOG PS 0-2で全身状態良好なⅣ期非小細胞肺癌患者に対する化学療法は,治療関連死を含む毒性のリスクはあるが生存期間を延長しQOLを改善することより行うよう勧められる。
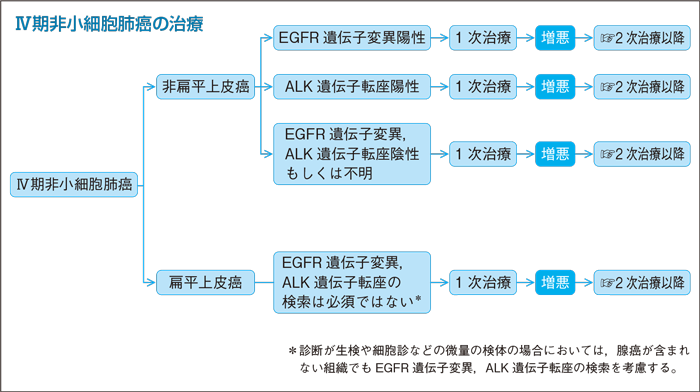
- 推 奨
- a.EGFR-TKI単剤を行うよう勧められる。(グレードA)
- b.1次治療で推奨される細胞障害性抗癌剤を行うよう勧められる。(グレードB)
*細胞障害性抗癌剤のレジメンについては非扁平上皮癌(EGFR遺伝子変異,ALK遺伝子転座陰性もしくは不明)の項におけるPS 0-1, 75歳未満の項目を参照すること。
- a・b.EGFR遺伝子変異陽性の進行非小細胞肺癌を対象にしたEGFR-TKI単剤(ゲフィチニブ,エルロチニブ,アファチニブ)とプラチナ製剤併用療法の比較第Ⅲ相試験が行われ,すべての試験において一貫してEGFR-TKI単剤のプラチナ製剤併用療法に対するPFSの有意な延長が報告され7)〜12),QOL指標の一部が改善することも示されている6)。以上より,PS 0-1, 75歳未満に対しては,EGFR-TKI単剤を推奨グレードAとし,1次治療で推奨される細胞障害性抗癌剤を推奨グレードBとした。
一方で,上述の試験においてEGFR-TKI単剤のプラチナ製剤併用療法に対するOSの差は示されていない13)14)。
大規模研究において,1次から3次治療のエルロチニブ単剤のPFSに有意差を認めないことが報告されている15)。
EGFR遺伝子変異陽性患者において,全治療期間におけるEGFR-TKI単剤と細胞障害性抗癌剤の投与順序に関しては,現時点で明確な結論はないが,EGFR遺伝子変異陽性患者に対してはEGFR-TKI単剤による治療を逸しないことが推奨される。
EGFR-TKIの主な毒性は,下痢,皮疹,爪囲炎,肝機能障害などであり,各々の薬剤で毒性の頻度や重症度が異なることが報告されているが,休薬や減量を行うことで長期間の服用が可能であることが示されている7)〜12)。
- 推 奨
- a.ゲフィチニブ単剤またはエルロチニブ単剤を行うよう勧められる。(グレードA)
- b.1次治療で推奨される細胞障害性抗癌剤を行うよう勧められる。(グレードB)
*細胞障害性抗癌剤のレジメンについては非扁平上皮癌(EGFR遺伝子変異,ALK遺伝子転座 陰性 もしくは不明)の項におけるPS 0-1, 75歳以上の項目を参照すること。
- a・b.75歳以上のEGFR遺伝子変異陽性進行非小細胞肺癌を対象とした国内でのゲフィチニブ単剤の第Ⅱ相試験において,ORR 74%,PFS 12.3カ月と若年者と同等の有効性と安全性が報告されている16)。エルロチニブ単剤については国内での第Ⅱ相試験において,75歳超と75歳以下で同等の有効性が示されている17)。アファチニブ単剤に関しては第Ⅲ相試験におけるサブグループ解析において,65歳以上は65歳未満と同等の有効性が報告されているが, 75歳以上の高齢者における安全性の検討は十分ではない11)12)。以上より,PS 0-1, 75歳以上の高齢者に対しては,ゲフィチニブ単剤またはエルロチニブ単剤を推奨グレードAとし,1次治療で推奨される細胞障害性抗癌剤を推奨グレードBとした。
EGFR-TKIの主な毒性は,下痢,皮疹,爪囲炎,肝機能障害などであり,各々の薬剤で毒性の頻度や重症度が異なることが報告されているが,休薬や減量を行うことで長期間の服用が可能であることが示されている7)〜12)。一方,高齢は間質性肺炎発症の危険因子であることが報告されており注意が必要である18)。
- 推 奨
- a.ゲフィチニブ単剤またはエルロチニブ単剤を行うよう勧められる。(グレードA)
- b.1次治療で推奨される細胞障害性抗癌剤を行うよう勧められる。(グレードB)
*細胞障害性抗癌剤のレジメンについては非扁平上皮癌(EGFR遺伝子変異,ALK遺伝子転座陰性もしくは不明)の項におけるPS 2の項目を参照すること。
- a・b.EGFR遺伝子変異陽性の進行非小細胞肺癌を対象としたエルロチニブ単剤とプラチナ製剤併用療法の2つの第Ⅲ相試験において,PS 2は各々7%,14%含まれておりPS 0-1と同等の有効性が示されている9)10)。また,ゲフィチニブ単剤はPS不良例に対する有効性が報告されている16)19)。アファチニブ単剤に関しては,PS 2に対する安全性・有効性の検討は十分ではない11)12)。以上より,PS 2に対しては,ゲフィチニブ単剤またはエルロチニブ単剤を推奨グレードAとし,1次治療で推奨される細胞障害性抗癌剤を推奨グレードBとした。
EGFR-TKIの主な毒性は,下痢,皮疹,爪囲炎,肝機能障害などであり,各々の薬剤で毒性の頻度や重症度が異なることが報告されているが,休薬や減量を行うことで長期間の服用が可能であることが示されている7)〜12)。一方,PS 2以上は間質性肺炎発症の危険因子であることが報告されており注意が必要である18)20)。
- 推 奨
- ゲフィチニブ単剤を行うよう考慮してもよい。(グレードC1)
PS 3-4に対しては細胞障害性抗癌剤の適応はない。
EGFR遺伝子変異陽性でPS 3-4が大多数を占める予後不良群を対象としてゲフィチニブ単剤の投与が行われ,80%近くでPSが改善し,ORR 66%,OS 17.8カ月,PFS 6.5カ月と極めて良好な治療効果が得られたとされた19)。一方でPS不良,男性,喫煙歴,既存の間質性肺炎,正常肺領域が少ないもの,心疾患を合併したものなどで間質性肺障害発症のリスクが高いことが報告されており18)20),慎重な検討も必要である。よって,PS 3-4に対してはゲフィチニブ単剤を推奨グレードC1とした。
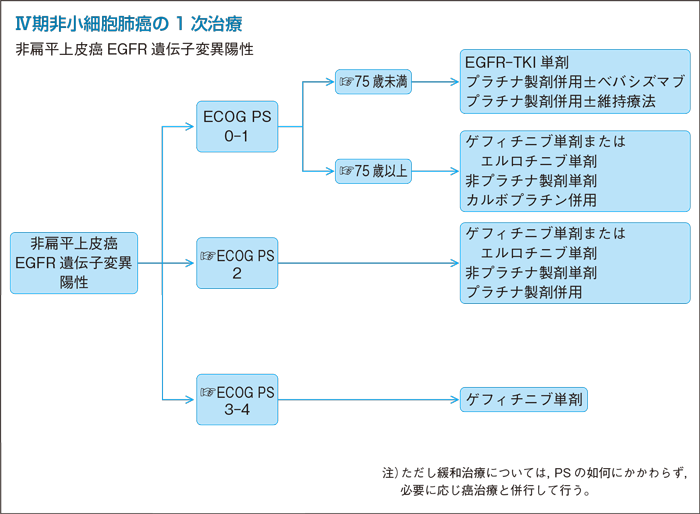
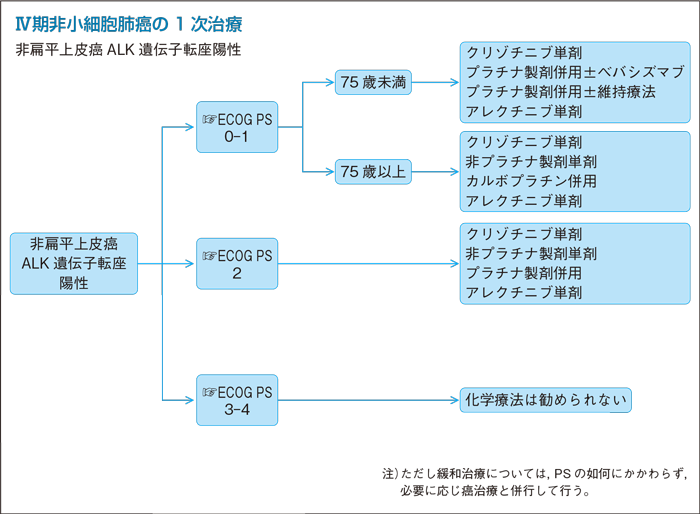
- 推 奨
- a.クリゾチニブ単剤を行うよう勧められる。(グレードA)
- b.1次治療で用いられる細胞障害性抗癌剤を行うよう勧められる。(グレードB)
- c.アレクチニブ単剤を行うよう考慮してもよい。(グレードC1)
*細胞障害性抗癌剤のレジメンについては非扁平上皮癌(EGFR遺伝子変異,ALK遺伝子転座陰性もしくは不明)の項におけるPS 0-1, 75歳未満/PS 0-1, 75歳以上/PS 2の項目を参照すること。
- c.アレクチニブ単剤を行うよう考慮してもよい。(グレードC1)
- a・b.1次治療としてALK遺伝子転座陽性の進行非小細胞肺癌を対象にしたクリゾチニブとプラチナ製剤併用療法の比較第Ⅲ相試験が行われ,PFSは10.9 vs 7.0 カ月(HR 0.454; 95%CI: 0.346-0.596; P<0.0001),ORRも74% vs 45%とクリゾチニブのプラチナ製剤併用療法に対するPFSの有意な延長が報告された21)。OSに関しては追跡調査中である。
- c.ALK融合遺伝子転座陽性の進行非小細胞肺癌患者を対象としてアレクチニブを投与する第Ⅰ-Ⅱ相試験が報告された。第Ⅱ相試験パートの46例の奏効率は93.5%と良好な成績が報告された22)。1次治療においては現在クリゾチニブ単剤との比較第Ⅲ相試験が行われているが,1次治療での安全性およびプラチナ製剤併用療法と比較したデータはなく,現時点では1次治療におけるアレクチニブ単剤の推奨グレードはC1とした。
以上より,クリゾチニブを推奨グレードA,アレクチニブを推奨グレードC1とし,1次治療で推奨される細胞障害性抗癌剤を推奨グレードBとした。
- 推 奨
- クリゾチニブ単剤は行うよう勧めるだけの根拠が明確ではない。(グレードC2)
PS 3-4に対する細胞障害性抗癌剤の適応はない。
EGFR遺伝子変異陽性・PS不良例においてゲフィチニブ単剤の有効性が示されたように,ALK遺伝子転座陽性・PS不良例においてもクリゾチニブ単剤の有効性が期待できる可能性はあるが,PS不良例に関してはこれまでの臨床試験で数例の参加が確認されるのみで有効性・安全性に関するデータは乏しい。クリゾチニブ単剤による死亡例(間質性肺障害・肝機能障害)も報告されており,PS不良例における安全性については慎重に検討していく必要がある。
以上より,ALK遺伝子転座陽性・PS 3-4に対するクリゾチニブ単剤は現時点では行うよう勧めるだけの根拠が明確ではなく,推奨グレードはC2とした。
- 推 奨
- a.1次治療で用いられる細胞障害性抗癌剤を行うよう勧められる。(グレードA)
*レジメンについてはPS 0-1, 75歳未満/PS 0-1, 75歳以上/PS 2の項目を参照すること。
- b.EGFR遺伝子変異不明の場合,EGFR-TKI単剤を行うよう勧めるだけの根拠が明確ではない。(グレードC2)
- a.非/軽喫煙者の進行肺腺癌を対象にしたゲフィチニブ単剤とCBDCA+PTXの第Ⅲ相試験においてEGFR遺伝子変異陽性と陰性でゲフィチニブ単剤のORRに著明な差が見られ(72% vs 1%),PFSにおいても同様の傾向が確認された(9.5カ月 vs 1.5カ月)23)24)。よってEGFR遺伝子変異陰性例に対するEGFR-TKI単剤は推奨されない。
ALK遺伝子転座陰性例に対するクリゾチニブ単剤の有効性は確認されておらず,推奨されない。
以上より,EGFR遺伝子変異陰性例・ALK遺伝子転座陰性例に対しては細胞障害性抗癌剤が推奨される。 - b.上記aのサブセット解析で,EGFR遺伝子変異不明例における6カ月以降のPFSはゲフィチニブ単剤がCBDCA+PTXより優れていたが,両群のPFS曲線が交差しており,この結果からゲフィチニブ単剤の優位性を判断することは困難である。また背景因子による選択のみでは約40%でEGFR遺伝子変異陰性であったことも留意する必要がある。
以上より,EGFR遺伝子変異不明例に対してはEGFR遺伝子変異陰性例と同様に細胞障害性抗癌剤を第一選択とすることを推奨し,EGFR-TKI単剤は行うよう勧められるだけの根拠が明確ではないため推奨グレードはC2とした。
- 推 奨
- <レジメン>
a.プラチナ製剤と第3世代以降の抗癌剤併用を行うよう勧められる。(グレードA)
b.ベバシズマブはリスクを考慮し,適応と考えられる非扁平上皮癌ではプラチナ製剤併用療法に追加するよう勧められる。(グレードB)
- <投与期間>
c.プラチナ製剤併用療法の投与期間は6コース以下とするよう勧められる。(グレードA)
- <維持療法>
d.PS 0-1に対するプラチナ製剤併用療法4コース後,病勢増悪を認めず毒性も忍容可能なものに対してPEMあるいはエルロチニブによるswitch maintenanceを考慮してもよい。(グレードC1)
e.PS 0-1に対するCDDP+PEM併用療法4コース後,病勢増悪を認めず毒性も忍容可能なものに対してPEMによるcontinuation maintenanceを行うよう勧められる。(グレードB)
- a.Baggstromらはプラチナ製剤併用の薬剤を第2世代と第3世代抗癌剤で比較したメタアナリシスにおいて,後者がORRで12%,1年生存率で6%優ると報告した2)。日本人においては,Oheらが4種類の第3世代抗癌剤とプラチナ製剤併用の第Ⅲ相試験の結果を報告しており,いずれの効果も同等であった25)。また,OkamotoらはCBDCA+S-1のCBDCA+PTXに対する非劣性を報告し,KatakamiらはCDDP+S-1のCDDP+DTXに対する非劣性を報告している26)27)。ヒト血清アルブミンとPTXを結合させたナノ粒子製剤であるnab-PTXとCBDCAの併用療法はCBDCA+PTXとの比較第Ⅲ相試験において,有意にORRの上昇を認めた(33.0% vs 25.0%)28)。各レジメンに固有の毒性プロファイルが報告されており,これらも踏まえて選択するべきと考えられる。
- b.SandlerらはCBDCA+PTXにベバシズマブを追加した第Ⅲ相試験を行い,併用群でORRの上昇,PFS(6.2カ月 vs 4.5カ月,HR 0.66, P<0.001)ならびにOS (12.3カ月 vs 10.3カ月,HR 0.79, P=0.003)の有意な延長を認めた29)。一方,CDDP+GEMにベバシズマブを追加した比較試験においては,PFSは有意に延長したがOSでは有意な延長を認めなかった30)。
本邦においてはCBDCA+PTXにベバシズマブを追加するランダム化第Ⅱ相試験(JO19907試験)が行われ,併用群においてCRRの上昇(60.7% vs 31.0%,P=0.0013),PFSの延長(6.9カ月 vs 5.9カ月,HR 0.61,P=0.0090) を認め,新たな毒性は認めなかったがOSについては有意な延長を認めなかった(22.8カ月 vs 23.4カ月,P=0.9526)31)。
上記の試験を含むメタアナリシスでは,プラチナ併用療法にベバシズマブを追加することでORRの上昇,PFSの延長が示されており,OSについても延長が認められたとする報告がある32)33)。一方で,ベバシズマブの併用でGrade3以上の毒性(蛋白尿,高血圧,出血性イベント,好中球減少,発熱性好中球減少,治療関連死)の有意な増加が報告されている32)〜34)。
出血リスクに関しては,扁平上皮癌や空洞を有する症例,大血管への浸潤や隣接を認めるもの,その他喀血・コントロール不能な高血圧,重篤な大血管病変や消化管における活動性出血の既往があるものなどが高リスク群と考えられており,ベバシズマブの投与に際してはその適応を十分に検討する必要がある34)。
ベバシズマブの投与についてはその薬剤の特性からプラチナ製剤併用療法の終了後,病勢増悪もしくは毒性中止まで単剤投与を継続する方法が一般的である29)〜34)。
- c.第3世代抗癌剤とプラチナ製剤との併用について,3コースもしくは4コースを6コースと比較し,いずれにおいても1年生存率やOSは同等で毒性は前者が軽いと報告された35)36)。一方,非扁平上皮癌に対するCDDP+PEMの優越性が示されたCDDP+GEMとの第Ⅲ相試験において,CDDP+PEM群の投与中央値は5コースであった37)。
- d.プラチナ製剤併用療法後のPEM,エルロチニブを用いたswitch maintenanceの第Ⅲ相試験でPFS・OSの延長が示された38)39)。しかしながら,両試験ともプラセボ群に対する2次療法以降でのクロスオーバーが少ないこと,すなわち,プラセボ群において2次治療以降に有効とされているPEM,エルロチニブが投与されていないことが問題とされている。
以上より,PEM・エルロチニブによるswitch maintenanceは選択肢の1つと考えられ,推奨グレードはC1とした。 - e.CDDP+PEM併用療法後のPEMを用いたcontinuation maintenanceの第Ⅲ相試験で,PFSの延長(4.1カ月 vs 2.8カ月,HR 0.62,P<0.0001),OSの延長(13.9カ月 vs 11.0カ月,HR 0.78,P=0.0195)が示された40)。QOL の低下は認めず,維持療法群において毒性の増強はみられたものの許容範囲内であった。以上より,PEMのcontinuation maintenanceの推奨グレードはBとした。
ベバシズマブの併用に関しては,CDDP+PEM+ベバシズマブ併用療法後にPEM+ベバシズマブ群とベバシズマブ単独群の第Ⅲ相試験が行われ,前者でPFSの有意な延長(7.4カ月 vs 3.7カ月,HR 0.48,P<0.0001)は認めたが,OSの有意な延長は認めなかった41)。
- 推 奨
a.暦年齢のみで化学療法の対象外とするべきではない。(グレードA)
- <レジメン>
b.第3世代抗癌剤単剤を行うよう勧められる。(グレードA)
c.カルボプラチン併用療法を考慮してもよい。(グレードC1)
d.ベバシズマブ併用は行うよう勧めるだけの根拠が明確ではない。(グレードC2)
- a.化学療法1次治療の第Ⅲ相試験と術後補助療法を対象とした検討では,65歳以上と以下で治療効果の差は認めず,暦年齢よりも日常生活自立度が予後に関係していた42)。また80歳以上でもPS良好のものは80歳以下と比べて効果・毒性に明らかな差は認めなかったと報告されている43)。
- b.高齢者においては緩和治療と比較してVNRが有効であること,VNRと比較してGEMが同様の有効性を示すことが確認されている44)45)。その後本邦で行われた第Ⅲ相試験(WJTOG9904試験)においてDTXはVNRに対し有意差は認めなかったもののPFS 5.5カ月,OS 14.3カ月と良好な結果を示した46)。以上より,高齢者に対する標準治療はDTXをはじめとした第3世代抗癌剤単剤と考えられる。
- c.高齢者に対するプラチナ製剤併用療法については第Ⅱ相試験や第Ⅲ相試験のサブセットから様々な報告がなされてきたが明確な結論には至っていない47)。
近年高齢者を対象とした第3世代抗癌剤単剤とプラチナ製剤併用療法を比較した第Ⅲ相試験が2編報告され,両試験とも登録された患者の多くが75歳以上であった。JCOG 0803/WJOG 4307L試験はweekly CDDP+DTXとDTXの比較であるが,この試験では中間解析において併用療法が単剤治療の成績を上回らないことが示され,試験中止となった48)。IFCT 0501試験はCBDCA+weekly PTXとGEMもしくはVNRの比較であり,PFS,OSにおける併用療法の優越性が示された(PFS;6.0カ月 vs 2.8カ月,P<0.0001,OS;10.3カ月 vs 6.2カ月,P<0.001)49)。しかしながらこの成績はbに述べた本邦での単剤治療の成績を大きく上回っているとはいえず,併用群における治療関連死が4.4%と高いなどの問題点が指摘されている。また投与量も本邦における標準的なものとは異なっており,データの解釈には注意を要する。
以上より,PS 0-1の75歳以上に対してCBDCA併用療法は選択肢の1つと考えられ,推奨グレードはC1とした。 - d.高齢者におけるプラチナ製剤併用療法+ベバシズマブについて,E4599試験におけるサブセット解析で70歳以上の高齢者では効果の上乗せは認められず,若年に比してGr 3以上の好中球減少・出血・蛋白尿が多かったとされている50)。米国における観察研究(ARIES)では70歳未満と70歳以上で効果は同等であったが,後者でGr 3以上の動脈血栓塞栓症が増える傾向にあり,80歳以上ではさらに高かった(70歳未満;1.2%,70歳以上;3.2%,80歳以上;4.1%)51)。一方,欧州を中心に施行された観察研究(SAiL)では,70歳未満と70歳以上で有効性は同等で毒性の増強は認めなかったと報告されている52)。
本邦においては75歳以上の高齢者におけるベバシズマブ併用療法の十分なデータはなく,有効性や安全性は確認されていない。以上より,現時点では高齢者に対するベバシズマブ併用を行うよう勧めるだけの根拠が明確ではなく,推奨グレードはC2とした。
- 推 奨
- <レジメン>
a.第3世代抗癌剤単剤を行うよう勧められる。(グレードA)
b.プラチナ製剤併用療法を考慮してもよい。(グレードC1)
c.第3世代抗癌剤併用は行うよう勧めるだけの根拠が明確ではない。(グレードC2)
d.ベバシズマブは行うよう勧めるだけの根拠が明確ではない。(グレードC2)
PS 2は多様な集団であり標準治療は定まっていない。
しかし,化学療法と緩和治療を比較したメタアナリシスのサブセットにおいて,PSに関わらず化学療法による生存期間の延長が認められている〔PS 2以上の場合,化学療法によって1年生存率にして6%(8%から14%)の改善〕1)。
- a.メタアナリシスにおいて第3世代抗癌剤(DTX・PTX・VNR・GEM)単剤治療は緩和治療に比して1年生存率で約7%の改善が示されているが2),この中にPS 2以上は約30%含まれていた。また,この解析でも取り上げられた3つの試験においてPS 2のサブセットの治療成績が明らかになっており,いずれもOSが延長する傾向が確認されている53)。
- b.PS2患者のサブセット解析が報告されており,CBDCA+PTXはPTX単剤に対して1年生存率で有意に上回っていた(18% vs 10%,HR 0.60,P=0.016)54)。PS 2に対するCBDCA+PTXとCDDP+GEMの比較では,OSはそれぞれ6.2,6.9カ月と良好であり,毒性に関しても忍容可能と考えられた55)。CBDCA+GEMとGEM単剤の比較が行われ,有意差は認められなかったものの併用群でOS(6.7カ月 vs 4.8カ月,P=0.49),PFS(4.1カ月 vs 3.0カ月,P=0.36)の延長傾向が示された56)。CBDCA+PEMと PEM単剤の第Ⅲ相試験が行われ,併用群でPFS(5.9カ月 vs 3.0カ月,HR 0.46,P<0.001),OS(9.1カ月 vs 5.6カ月,HR 0.57,P=0.001)の有意な延長が認められた。毒性に関しては併用群で貧血や好中球減少の頻度が高く,3.9%の治療関連死が認められた57)。
以上より,毒性が耐用可能と思われるPS 2に対してはプラチナ製剤併用療法を考慮してもよいが,PS 2に関するエビデンスは少なく,その殆どがCBDCA併用レジメン,もしくは通常より減量した用量が用いられていることに注意が必要であり,推奨グレードはC1とした。 - c.PS 2に対する第3世代抗癌剤併用のエビデンスは少ない。weekly DTXとDTX+GEMの比較第Ⅱ相試験が行われ,約35%を占めたPS 2患者において併用によるOS延長は認めず(2.9カ月 vs 3.8カ月,P=0.62),毒性が増強していた58)。よって,行うよう勧めるだけの根拠が明確ではなく推奨グレードはC2とした。
- d.ベバシズマブ併用の臨床試験ならびに観察研究においてその大半がPS 0-1であり,PS 2に対するベバシズマブの安全性や有効性に関してのデータは少ない29)〜34)53)。よって,PS 2に対するベバシズマブは行うよう勧めるだけの根拠が明確ではなく,推奨グレードはC2とした。
- 推 奨
- 化学療法は行わないよう勧められる。(グレードD)
PS 3-4に対する細胞障害性抗癌剤の適応はない。
PS不良や合併症のため化学療法の適応とならない進行非小細胞肺癌に対してエルロチニブ単剤と緩和治療の第Ⅲ相試験が行われた59)。患者背景として年齢中央値77歳,PS 3が30%を占め,EGFR遺伝子変異については陰性,不明がそれぞれ52%,46%であった。この試験においてOSの延長がみられなかったことから,EGFR遺伝子変異陰性もしくは不明のPS 3-4についてEGFR-TKI単剤は推奨されない。
ALK遺伝子転座陰性例に対するクリゾチニブ単剤の有効性は確認されておらず,推奨されない。
以上より,EGFR遺伝子変異,ALK遺伝子転座陰性,もしくは不明の非扁平上皮癌でPS 3-4については化学療法は勧められない。
- 推 奨
- <レジメン>
a.プラチナ製剤と第3世代以降の抗癌剤併用を行うよう勧められる。(グレードA)
b.PEMは行わないよう勧められる。(グレードD)
c.ベバシズマブは行わないよう勧められる。(グレードD)
- <投与期間>
d.プラチナ製剤併用療法の投与期間は基本的に6コース以下とすることが勧められる。(グレードA)
- <維持療法>
e.PS 0-1に対するプラチナ製剤併用療法4コース後,病勢増悪を認めず毒性も忍容可能なものに対してswitch maintenance, continuation maintenanceともに行うよう勧めるだけの根拠が明確ではない。(グレードC2)
- a.プラチナ製剤併用の薬剤を第2世代と第3世代抗癌剤で比較したメタアナリシスにおいて,後者がORRで12%,1年生存率で6%優ると報告した2)。日本人においては,4種類の第3世代抗癌剤とプラチナ製剤併用の第Ⅲ相試験の結果が報告されており,いずれの効果も同等であった25)。またCBDCA+S-1のCBDCA+PTXに対する非劣性が報告され,CDDP+S-1のCDDP+DTXに対する非劣性も報告されている26)27)。ヒト血清アルブミンとPTXを結合させたナノ粒子製剤であるnab-PTXとCBDCAの併用療法は,CBDCA+PTXとの比較第Ⅲ相試験において,有意にORRの上昇を認めた(33.0% vs 25.0%)28)。各レジメンに固有の毒性プロファイルが報告されており,これらも踏まえて選択するべきと考えられる。
- b.CDDP+PEMとCDDP+GEMの第Ⅲ相試験が行われ,全体では同等の効果であったが組織型による差が認められた。非扁平上皮癌においてはCDDP+PEM群でOS延長(11.8カ月 vs 10.4カ月,HR 0.81,P=0.005)を認めたが,扁平上皮癌では,逆にCDDP+PEM群でPFS(4.4カ月 vs 5.5カ月,HR 1.36,P=0.002),OS(9.4カ月 vs 10.8カ月,HR 1.23,P=0.05)ともに劣っていた37)。組織型によるPEMの効果の違いについてはPEM単剤を用いた第Ⅲ相試験も併せて解析され,上記同様の傾向が確認されている60)。以上より,PEMは扁平上皮癌に対して行わないよう勧められる。
- c.ベバシズマブの第Ⅱ相試験においてGrade 3以上の肺胞出血が9.1%に認められ,出血リスクに関する検討が行われた。現在のところ,扁平上皮癌や空洞を有する症例,大血管への浸潤や隣接を認めるもの,その他喀血・コントロール不能な高血圧,重篤な大血管病変や消化管における活動性出血の既往があるものなどが高リスク群と考えられており34),ベバシズマブは扁平上皮癌に対して行わないよう勧められる。
- d.第3世代抗癌剤とプラチナ製剤との併用について,3コースもしくは4コースと6コースが比較され,いずれにおいても1年生存率やOSは同等で毒性は前者が軽いと報告された35)36)。一方,非扁平上皮癌に対するCDDP+PEMの優越性が示されたCDDP+GEMとの第Ⅲ相試験において,CDDP+PEM群の投与中央値は5コースであった37)。
- 推 奨
a.暦年齢のみで化学療法の対象外とするべきではない。(グレードA)
- <レジメン>
b.第3世代抗癌剤単剤を行うよう勧められる。(グレードA)
c.カルボプラチン併用療法を考慮してもよい。(グレードC1)
d.PEMは行わないよう勧められる。(グレードD)
e.ベバシズマブは行わないよう勧められる。(グレードD)
- a.化学療法1次治療の第Ⅲ相試験と術後補助療法を対象とした検討では,65歳以上と以下で治療効果の差は認めず,暦年齢よりも日常生活自立度が予後に関係していた42)。また80歳以上でもPS良好のものは80歳以下と比べて効果・毒性に明らかな差は認められなかったと報告されている43)。
- b.高齢者においては緩和治療と比較してVNRが有効であること,VNRと比較してGEMが同様の有効性を示すことが確認されている44)45)。その後本邦で行われた第Ⅲ相試験においてDTXはVNRに対し有意差は認めなかったもののPFS 5.5カ月,OS 14.3カ月と良好な結果を示した46)。以上より,高齢者に対する標準治療はDTXをはじめとした第3世代抗癌剤単剤と考えられる。
- c.高齢者に対するプラチナ製剤併用療法については第Ⅱ相試験や第Ⅲ相試験のサブセットから様々な報告がなされてきたが明確な結論には至っていない47)。
近年高齢者を対象とした第3世代抗癌剤単剤とプラチナ製剤併用療法を比較した第Ⅲ相試験が2編報告され,両試験とも登録された患者の多くが75歳以上であった。weekly CDDP+DTXとDTXの比較では,中間解析において併用療法が単剤治療の成績を上回らないことが示され,試験中止となった48)。CBDCA+weekly PTXとGEMもしくはVNRの比較では,PFS,OSにおける併用療法の優越性が示された(PFS;6.0カ月 vs 2.8カ月,P<0.0001,OS;10.3カ月 vs 6.2カ月,P<0.001)49)。しかしながらこの成績はbに述べた本邦での単剤治療の成績を大きく上回っているとはいえず,併用群における治療関連死が4.4%と高いなどの問題点が指摘されている。また投与量も本邦における標準的なものとは異なっており,データの解釈には注意を要する。
以上より,PS 0-1,75歳以上に対してCBDCA併用療法は選択肢の1つと考えられ,推奨グレードはC1とした。 - d.CDDP+PEMとCDDP+GEMの第Ⅲ相試験が行われ,全体では同等の効果であったが組織型による差が認められた。非扁平上皮癌においてはCDDP+PEM群でOS延長(11.8カ月 vs 10.4カ月,HR 0.81,P=0.005)を認めたが,扁平上皮癌では,逆にCDDP+PEM群でPFS(4.4カ月 vs 5.5カ月,HR 1.36,P=0.002),OS(9.4カ月 vs 10.8カ月,HR 1.23,P=0.05)ともに劣っていた37)。組織型によるPEMの効果の違いについてはPEM単剤を用いた第Ⅲ相試験も併せて解析され,上記同様の傾向が確認されている60)。以上より,PEMは扁平上皮癌に対して行わないよう勧められる。
- e.ベバシズマブの第Ⅱ相試験においてGrade 3以上の肺胞出血が9.1%に認められ,出血リスクに関する検討が行われた。現在のところ,扁平上皮癌や空洞を有する症例,大血管への浸潤や隣接を認めるもの,その他喀血・コントロール不能な高血圧,重篤な大血管病変や消化管における活動性出血の既往があるものなどが高リスク群と考えられており34),ベバシズマブは扁平上皮癌に対して行わないよう勧められる。
- 推 奨
- <レジメン>
a.第3世代抗癌剤単剤を行うよう勧められる。(グレードA)
b.プラチナ製剤併用療法を考慮してもよい。(グレードC1)
c.第3世代抗癌剤併用は行うよう勧めるだけの根拠が明確ではない。(グレードC2)
d.PEMは行わないよう勧められる。(グレードD)
e.ベバシズマブは行わないよう勧められる。(グレードD)
PS 2は多様な集団であり標準治療は定まっていない。
しかし化学療法と緩和治療を比較したメタアナリシスのサブセットにおいて,PSにかかわらず化学療法による生存期間の延長が認められている〔PS 2以上の場合,化学療法によって1年生存率にして6%(8%から14%)の改善〕1)。
- a.メタアナリシスにおいて第3世代抗癌剤(DTX・PTX・VNR・GEM)単剤治療は緩和治療に比して1年生存率で約7%の改善が示されているが2),この中にPS 2以上は約30%含まれていた。また,この解析でも取り上げられた3つの試験においてPS 2のサブセットの治療成績が明らかになっており,いずれもOSが延長する傾向が確認されている53)。
- b.PS 2患者のサブセット解析が報告されており,CBDCA+PTXはPTX単剤に対して1年生存率で有意に上回っていた(18% vs 10%,HR 0.60,P=0.016)54)。PS 2に対するCBDCA+PTXとCDDP+GEMの比較が行われ,OSはそれぞれ6.2,6.9カ月と良好であり,毒性に関しても忍容可能と考えられた55)。CBDCA+GEMとGEM単剤の比較が行われ,有意差は認めなかったものの併用群でOS(6.7カ月 vs 4.8カ月,P=0.49),PFS(4.1カ月 vs 3.0カ月,P=0.36)の延長傾向が示された56)。CBDCA+PEMと PEM単剤の第Ⅲ相試験が行われ,併用群でPFS (5.9カ月 vs 3.0カ月, HR 0.46, P<0.001), OS(9.1カ月 vs 5.6カ月, HR 0.57, P=0.001)の有意な延長を認めた。毒性に関しては併用群で貧血や好中球減少の頻度が高く,3.9%の治療関連死が認められた57)。
以上より,毒性が耐用可能と思われるPS 2に対してはプラチナ製剤併用療法を考慮してもよい。しかしながらPS 2に関するエビデンスは少なく,その殆どがCBDCA併用レジメン,もしくは通常より減量した用量が用いられていることに注意が必要であり,推奨グレードはC1とした。 - c.PS 2に対する第3世代抗癌剤併用のエビデンスは少ない。weekly DTXとDTX+GEMの比較第Ⅱ相試験が行われ,約35%を占めたPS 2患者において併用によるOS延長は認めず(2.9カ月 vs 3.8カ月,P=0.62),毒性が増強していた58)。よって,行うよう勧めるだけの根拠が明確ではなく推奨グレードはC2とした。
- d.CDDP+PEMとCDDP+GEMの第Ⅲ相試験が行われ,全体では同等の効果であったが組織型による差が認められた。非扁平上皮癌においてはCDDP+PEM群でOS延長(11.8カ月 vs 10.4カ月,HR 0.81,P=0.005)を認めたが,扁平上皮癌では,逆にCDDP+PEM群でPFS(4.4カ月 vs 5.5カ月,HR 1.36,P=0.002),OS(9.4カ月 vs 10.8カ月,HR 1.23,P=0.05)ともに劣っていた37)。組織型によるPEMの効果の違いについてはPEM単剤を用いた第Ⅲ相試験も併せて解析され,上記同様の傾向が確認されている60)。以上より,PEMは扁平上皮癌に対して行わないよう勧められる。
- e.ベバシズマブの第Ⅱ相試験においてGrade 3以上の肺胞出血が9.1%に認められ,出血リスクに関する検討が行われた。現在のところ,扁平上皮癌や空洞を有する症例,大血管への浸潤や隣接を認めるもの,その他喀血・コントロール不能な高血圧,重篤な大血管病変や消化管における活動性出血の既往があるものなどが高リスク群と考えられており34),ベバシズマブは扁平上皮癌に対して行わないよう勧められる。
- 推 奨
- 化学療法は行わないよう勧められる。(グレードD)
PS 3-4に対する細胞障害性抗癌剤の適応はない。
PS不良や合併症のため化学療法の適応とならない進行非小細胞肺癌に対して,エルロチニブ単剤と緩和治療の第Ⅲ相試験が行われた59)。患者背景として扁平上皮癌が40%,PS 3が30%を占めており,この試験においてOSの延長はみられなかった。
以上より扁平上皮癌,PS 3-4については化学療法は勧められない。
- 1)Non-Small Cell Lung Cancer Collaborative Group. Chemotherapy and supportive care versus supportive care alone for advanced non-small cell lung cancer. Cochrane Database Syst Rev. 2010; 12(5): CD007309. (I)
- 2)Baggstrom MQ, Stinchcombe TE, Fried DB, et al. Third-generation chemotherapy agents in the treatment of advanced non-small cell lung cancer: a meta-analysis. J Thorac Oncol. 2007; 2(9): 845-53. (I)
- 3)Fujiwara Y, Hotta K, Di Maio M, et al. Time trend in treatment-related deaths of patients with advanced non-small-cell lung cancer enrolled into phase III trials of systemic treatment. Ann Oncol. 2011; 22(2): 376-82. (I)
- 4)Anderson H, Hopwood P, Sstephens RJ, et al. Gemcitabine plus best supportive care (BSC) vs BSC in inoperable non-small cell lung cancer--a randomized trial with quality of life as the primary outcome. UK NSCLC Gemcitabine Group. Non-Small Cell Lung Cancer. Br J Cancer. 2000; 83(4): 447-53. (II)
- 5)Sederholm C, Hillerdal G, Lamberg K, et al. Phase III trial of gemcitabine plus carboplatin versus single-agent gemcitabine in the treatment of locally advanced or metastatic non-small-cell lung cancer: the Swedish Lung Cancer Study Group. J Clin Oncol. 2005; 23(33): 8380-8. (II)
- 6)Oizumi S, Kobayashi K, Inoue A, et al. Quality of life with gefitinib in patients with EGFR-mutated non-small cell lung cancer: quality of life analysis of North East Japan Study Group 002 Trial. Oncologist. 2012; 17(6): 863-70. (II)
- 7)Mitsudomi T, Morita S, Yatabe Y, et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor (WJTOG3405): an open label, randomised phase 3 trial. Lancet Oncol. 2010; 11(2): 121-8. (II)
- 8)Maemondo M, Inoue A, Kobayashi K, et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med. 2010; 362(25): 2380-8. (II)
- 9)Zhou C, Wu YL, Chen G, et al. Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer (OPTIMAL. CTONG-0802): a multicentre, open-label, randomised phase 3 study. Lancet Oncol. 2011; 12(8): 735-42. (II)
- 10)Rosell R, Carcereny E, Gervais R, et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer (EURTAC): a multicentre, open-label, randomised phase 3 trial. Lancet Oncol. 2012; 13(3): 239-46. (II)
- 11)Sequist LV, Yang JC, Yamamoto N, et al. Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol. 2013; 31(27): 3327-34. (II)
- 12)Wu YL, Zhou C, Hu CP, et al. Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations(LUX-Lung 6): an open-label, randomised phase 3 trial. Lancet Oncol. 2014; 15(2):213-22. (II)
- 13)Inoue A, Kobayashi K, Maemondo M, et al. Updated overall survival results from a randomized phase III trial comparing gefitinib with carboplatin-paclitaxel for chemo-naïve non-small cell lung cancer with sensitive EGFR gene mutations (NEJ002). Ann Oncol. 2013; 24(1):54-9. (II)
- 14)Zhou C, Wu YL, Liu X, et al. Overall survival (OS) results from OPTIMAL (CTONG0802), a phase III trial of erlotinib (E) versus carboplatin plus gemcitabine (GC) as first-line treatment for Chinese patients with EGFR mutation-positive advanced non-small cell lung cancer (NSCLC). J Clin Oncol. 2012; 30 (suppl; abstr 7520). (II)
- 15)Rosell R, Moran T, Queralt C, et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J Med. 2009; 361(10): 958-67. (III)
- 16)Maemondo M, Minegishi Y, Inoue A, et al. First-line gefitinib in patients aged 75 or older with advanced non-small cell lung cancer harboring epidermal growth factor receptor mutations: NEJ 003 study. J Thorac Oncol. 2012; 7(9): 1417-22. (III)
- 17)Goto K, Nishio M, Yamamoto N, et al. A prospective, phase II,open-label study(JO22903)of first-line erlotinib in Japanese patients with epidermal growth factor receptor(EGFR) mutation-positive advanced non-small-cell lung cancer(NSCLC). Lung Cancer. 2013; 82(1): 109-14. (III)
- 18)Kudoh S, Kato H, Nishiwaki Y, et al. Interstitial lung disease in Japanese patients with lung cancer: a cohort and nested case-control study. Am J Respir Crit Care Med. 2008; 177(12): 1348-57. (IV)
- 19)Inoue A, Kobayashi K, Usui K, et al. First-line gefitinib for patients with advanced non-small-cell lung cancer harboring epidermal growth factor receptor mutations without indication for chemotherapy. J Clin Oncol. 2009; 27(9): 1394-400. (III)
- 20)Ando M, Okamoto I, Yamamoto N, et al. Predictive factors for interstitial lung disease, antitumor response, and survival in non-small-cell lung cancer patients treated with gefitinib. J Clin Oncol. 2006; 24(16): 2549-56. (IV)
- 21)Mok T, Kim DW, Wu YK, et al. First-line crizotinib versus pemetrexed-cisplatin or pemetrexed-carboplatin in patients with advanced ALK-positive Non-squamous cell lung cancer: results of a phase III study (PROFILE 1014). J Clin Oncol. 32, 2014 (suppl; abstr 8002).(II)
- 22)Seto T, Kiura K, Nishio M, et al. CH5424802(RO5424802)for patients with ALK-rearranged advanced non-small-cell lung cancer(AF-001JP study): a single-arm, open-label, phase 1-2 study. Lancet Oncol. 2013; 14(7): 590-8. (III)
- 23)Mok TS, Wu YL, Thongprasert S, et al. Gefitinib or carboplatin-paclitaxel in pulmonary adenocarcinoma. N Engl J Med. 2009; 361(10): 947-57. (II)
- 24)Fukuoka M, Wu YL, Thongprasert S, et al. Biomarker analyses and final overall survival results from a phase III, randomized, open-label, first-line study of gefitinib versus carboplatin/paclitaxel in clinically selected patients with advanced non-small-cell lung cancer in Asia (IPASS). J Clin Oncol. 2011; 29(21): 2866-74. (II)
- 25)Ohe Y, Ohashi Y, Kubota K, et al. Randomized phase III study of cisplatin plus irinotecan versus carboplatin plus paclitaxel, cisplatin plus gemcitabine, and cisplatin plus vinorelbine for advanced non-small-cell lung cancer: Four-Arm Cooperative Study in Japan. Ann Oncol. 2007; 18(2): 317-23. (II)
- 26)Okamoto I, Yoshioka H, Morita S, et al. Phase III trial comparing oral S-1 plus carboplatin with paclitaxel plus carboplatin in chemotherapy-naïve patients with advanced non-small-cell lung cancer: results of a west Japan oncology group study. J Clin Oncol. 2010; 28(36): 5240-6. (II)
- 27)Katakami N, Gemma A, Sakai H, at el. Randomized phase III trial of S-1 plus cisplatin versus docetaxel plus cisplatin for advanced non-small-cell lung cancer (TCOG0701). J Clin Oncol. 30, 2012(suppl; abstr 7515). (II)
- 28)Socinski MA, Bondarenko I, Karaseva NA, et al. Weekly nab-paclitaxel in combination with carboplatin versus solvent-based paclitaxel plus carboplatin as first-line therapy in patients with advanced non-small-cell lung cancer: final results of a phase III trial. J Clin Oncol. 2012; 30(17): 2055-62. (II)
- 29)Sandler A, Gray R, Perry MC, et al. Paclitaxel-carboplatin alone or with bevacizumab for non-small-cell lung cancer. N Engl J Med. 2006; 355(24): 2542-50. (II)
- 30)Reck M, von Pawel J, Zatloukal P, et al. Overall survival with cisplatin-gemcitabine and bevacizumab or placebo as first-line therapy for nonsquamous non-small-cell lung cancer: results from a randomised phase III trial (AVAiL). Ann Oncol. 2010; 21(9): 1804-9. (II)
- 31)Niho S, Kunitoh H, Nokihara H, et al; JO19907 Study Group. Randomized phase II study of first-line carboplatin-paclitaxel with or without bevacizumab in Japanese patients with advanced non-squamous non-small-cell lung cancer. Lung Cancer. 2012; 76(3): 362-7. (II)
- 32)Lima AB, Macedo LT, Sasse AD. Addition of bevacizumab to chemotherapy in advanced non-small cell lung cancer: a systematic review and meta-analysis. PLoS One. 2011; 6(8): e22681. (I)
- 33)Soria JC, Mauguen A, Reck M, et al. Systematic review and meta-analysis of randomised, phase II/III trials adding bevacizumab to platinum-based chemotherapy as first-line treatment in patients with advanced non-small-cell lung cancer. Ann Oncol. 2013; 24(1): 20-30. (I)
- 34)Sandler AB, Schiller JH, Gray R, et al. Retrospective evaluation of the clinical and radiographic risk factors associated with severe pulmonary hemorrhage in first-line advanced, unresectable non-small-cell lung cancer treated with Carboplatin and Paclitaxel plus bevacizumab. J Clin Oncol. 2009; 27(9): 1405-12. (IV)
- 35)von Plessen C, Bergman B, Andressen O, et al. Palliative chemotherapy beyond three courses conveys no survival or consistent quality-of-life benefits in advanced non-small-cell lung cancer. Br J Cancer. 2006; 95(8): 966-73. (II)
- 36)Park JO, Kim SW, Ahn JS, et al. Phase III trial of two versus four additional cycles in patients who are nonprogressive after two cycles of platinum-based chemotherapy in non small-cell lung cancer. J Clin Oncol. 2007; 25(33): 5233-9. (II)
- 37)Scagliotti GV, Parikh P, von Pawel J, et al. Phase III study comparing cisplatin plus gemcitabine with cisplatin plus pemetrexed in chemotherapy-naive patients with advanced-stage non-small-cell lung cancer. J Clin Oncol. 2008; 26(21): 3543-51. (II)
- 38)Ciuleanu T, Brodowicz T, Zielinski C, et al. Maintenance pemetrexed plus best supportive care versus placebo plus best supportive care for non-small-cell lung cancer: a randomised, double-blind, phase 3 study. Lancet. 2009; 374(9699): 1432-40. (II)
- 39)Cappuzzo F, Ciuleanu T, Stelmakh L, et al. Erlotinib as maintenance treatment in advanced non-small-cell lung cancer: a multicentre, randomised, placebo-controlled phase 3 study. Lancet Oncol. 2010; 11(6): 521-9. (II)
- 40) Paz-Ares LG, de Marinis F, Dediu M, et al. PARAMOUNT: Final overall survival results of the phase III study of maintenance pemetrexed versus placebo immediately after induction treatment with pemetrexed plus cisplatin for advanced nonsquamous non-small-cell lung cancer. J Clin Oncol. 2013; 31(23): 2895-902. (II)
- 41) Barlesi F, Scherpereel A, Gorbunova V, et al. Maintenance bevacizumab-pemetrexed after first-line cisplatin-pemetrexed-bevacizumab for advanced nonsquamous nonsmall-cell lung cancer: updated survival analysis of the AVAPERL(MO22089)randomized phase III trial. Ann Oncol. 2014; 25(5):1044-52.(II)
- 42)Maione P, Perrone F, Gallo C, et al. Pretreatment quality of life and functional status assessment significantly predict survival of elderly patients with advanced non-small-cell lung cancer receiving chemotherapy: a prognostic analysis of the multicenter Italian lung cancer in the elderly study. J Clin Oncol. 2005; 23(28): 6865-72. (IV)
- 43)Hesketh PJ, Lilenbaum RC, Chansky K, et al. Chemotherapy in patients > or = 80 with advanced non-small cell lung cancer: combined results from SWOG 0027 and LUN 6. J Thorac Oncol. 2007; 2(6): 494-8. (IV)
- 44)The Elderly Lung Cancer Vinorelbine Italian Study Group. Effects of vinorelbine on quality of life and survival of elderly patients with advanced non-small-cell lung cancer. J Natl Cancer Inst. 1999;91(1):66-72. (II)
- 45)Gridelli C, Perrone F, Gallo C, et al. Chemotherapy for elderly patients with advanced non-small-cell lung cancer: the Multicenter Italian Lung Cancer in the Elderly Study (MILES) phase III randomized trial. J Natl Cancer Inst. 2003; 95(5): 362-72. (II)
- 46)Kudoh S, Takeda K, Nakagawa K, et al. Phase III study of docetaxel compared with vinorelbine in elderly patients with advanced non-small-cell lung cancer: results of the West Japan Thoracic Oncology Group Trial (WJTOG 9904). J Clin Oncol. 2006; 24(22): 3657-63. (II)
- 47)Belani CP, Fossella F. Elderly subgroup analysis of a randomized phase III study of docetaxel plus platinum combinations versus vinorelbine plus cisplatin for first-line treatment of advanced nonsmall cell lung carcinoma (TAX 326). Cancer. 2005; 104(12): 2766-74. (IV)
- 48)Abe T, Yokoyama K, Takeda K, et al. Randomized phase III trial comparing weekly docetaxel (D)-cisplatin (P) combination with triweekly D alone in elderly patients (pts) with advanced non-small cell lung cancer (NSCLC): An intergroup trial of JCOG0803/WJOG4307L. J Clin Oncol. 2011; 29 (suppl; abstr 7509). (II)
- 49)Quoix E, Zalcman G, Oster JP, et al. Carboplatin and weekly paclitaxel doublet chemotherapy compared with monotherapy in elderly patients with advanced non-small-cell lung cancer: IFCT-0501 randomised, phase 3 trial. Lancet. 2011; 378(9796): 1079-88. (II)
- 50)Ramalingam SS, Dahlberg SE, Langer CJ, et al. Outcomes for elderly, advanced-stage non small-cell lung cancer patients treated with bevacizumab in combination with carboplatin and paclitaxel: analysis of Eastern Cooperative Oncology Group Trial 4599. J Clin Oncol. 2008; 26(1): 60-5. (IV)
- 51)Wozniak AJ, Garst J, Jahanzeb M, et al. Clinical outcomes (CO) for special populations of patients (pts) with advanced non-small cell lung cancer (NSCLC): Results from ARIES, a bevacizumab (BV) observational cohort study (OCS). J Clin Oncol. 28:15s, 2010(suppl; abstr 7618) (IV)
- 52)Laskin J, Crinò L, Felip E, et al. Safety and efficacy of first-line bevacizumab plus chemotherapy in elderly patients with advanced or recurrent nonsquamous non-small cell lung cancer: safety of avastin in lung trial (MO19390). J Thorac Oncol. 2012; 7(1): 203-11. (IV)
- 53)Gridelli C, Ardizzoni A, Chevalier TL, et al. Treatment of advanced non-small-cell lung cancer patients with ECOG performance status 2: results of an European Experts Panel. Ann Oncol. 2004;15(3):419-26. (IV)
- 54)Lilenbaum RC, Herndon JE 2nd, List MA, et al. Single-agent versus combination chemotherapy in advanced non-small-cell lung cancer: the cancer and leukemia group B (study 9730). J Clin Oncol. 2005; 23(1): 190-6. (IV)
- 55)Langer C, Li S, Schiller J, et al. Randomized phase II trial of paclitaxel plus carboplatin or gemcitabine plus cisplatin in Eastern Cooperative Oncology Group performance status 2 non-small-cell lung cancer patients: ECOG 1599. J Clin Oncol. 2007; 25(4): 418-23. (II)
- 56)Kosmidis PA, Dimopoulos MA, Syrigos K, et al. Gemcitabine versus gemcitabine-carboplatin for patients with advanced non-small cell lung cancer and a performance status of 2: a prospective randomized phase II study of the Hellenic Cooperative Oncology Group. J Thorac Oncol. 2007; 2(2): 135-40. (II)
- 57)Zukin M, Barrios CH, Pereira JR, et al. Randomized phase III trial of single-agent pemetrexed versus carboplatin and pemetrexed in patients with advanced non-small-cell lung cancer and Eastern Cooperative Oncology Group performance status of 2. J Clin Oncol. 2013; 31(23): 2849-53. (II)
- 58)Hainsworth JD, Spigel DR, Farley C, et al. Weekly docetaxel versus docetaxel/gemcitabine in the treatment of elderly or poor performance status patients with advanced nonsmall cell lung cancer: a randomized phase 3 trial of the Minnie Pearl Cancer Research Network. Cancer. 2007; 110(9): 2027-34. (II)
- 59)Lee SM, Khan I, Upadhyay S, et al. First-line erlotinib in patients with advanced non-small-cell lung cancer unsuitable for chemotherapy (TOPICAL): a double-blind, placebo-controlled, phase 3 trial. Lancet Oncol. 2012; 13(11): 1161-70. (II)
- 60)Scagliotti G, Hanna N, Fossella F, et al. The differential efficacy of pemetrexed according to NSCLC histology: a review of two Phase III studies. Oncologist. 2009; 14(3): 253-63. (IV)
| CDDP | 75mg/m2, day1 | q3w |
| PEM | 500mg/m2, day1 | |
| 維持療法:PEM 500mg/m2, day1 | ||
| ※PEMの投与に際しては下記ビタミンの補充を行う ①葉酸:投与の7日以上前から葉酸として1日1回0.5mgを連日経口投与する。なお,本剤の投与を中止または終了する場合には,本剤最終投与日から22日目まで可能な限り葉酸を投与する。 ②ビタミンB12:初回投与の少なくとも7日前に,ビタミンB12として1回1mgを筋肉内投与する。その後,本剤投与期間中及び投与中止後22日目まで9週ごと(3コースごと)に1回投与する。 |
||
| CDDP | 80mg/m2, day1 | q3w |
| DTX | 60mg/m2, day1 | |
| CDDP | 80mg/m2, day1 | q3w |
| GEM | 1000mg/m2, day1, 8 | |
| CDDP | 80mg/m2, day1 | q3w |
| VNR | 25mg/m2, day1, 8 | |
| CDDP | 80mg/m2, day1 | q4w |
| CPT-11 | 60mg/m2, day1, 8, 15 | |
| CDDP | 60mg/m2, day8 | q4-5w |
| S-1 | 40mg/m2 , 1日2回, day1-21 | |
| CBDCA | (AUC=6), day1 | q3w |
| PTX | 200mg/m2, day1 | |
| PTX投与30分前までにデキサメサゾン,H1,H2 blockerの前投薬を行う。 | ||
| CBDCA | (AUC=5), day1 | q3w |
| GEM | 1000mg/m2, day1, 8 | |
| CBDCA | (AUC=5), day1 | q3w |
| S-1 | 40mg/m2 , 1日2回, day1-14 | |
| CBDCA | (AUC=6), day1 | q3w |
| nab-PTX | 100mg/m2, day1, 8, 15 | |
- 増悪しなければ上記を6コース以内で繰り返す。
- 維持療法を行う場合はプラチナ製剤併用を4コースで終了し,病勢増悪を認めず,毒性が忍容可能な場合に(プラチナ製剤を含まない)単剤化学療法に移行する。
| CBDCA | (AUC=6) ,day1 | q3w |
| PTX | 200mg/m2, day1 | |
| Bevacizumab | 15mg/kg, day1 | |
| PTX投与30分前までにデキサメサゾン,H1,H2 blockerの前投薬を行う。 | ||
- 増悪しなければ上記を6コース以内で繰り返す。
- ベバシズマブについてはプラチナ製剤併用療法の終了後,病勢増悪もしくは毒性中止まで単剤投与を継続する。
| DTX | 60mg/m2, day1 | q3w |
| GEM | 1000mg/m2, day1, 8, 15 | q4w |
| VNR | 25mg/m2, day1, 8 | q3w |
| Gefitinib | 250mg/日 1錠 | 1日1回 |
| Erlotinib | 150mg/日 1錠 | 1日1回 |
| Afatinib | 40mg/日 1錠 | 1日1回 |
| Crizotinib | 500mg/日 1回250mg | 1日2回 |
| Alectinib | 600mg/日 (40mg)7錠,(20mg)1錠 | 1日2回 |