6

| プラチナ製剤 | シスプラチンとカルボプラチンの総称 | |
| 第1・2世代のEGFR-TKI | ゲフィチニブ・エルロチニブ・アファチニブの総称 | |
| ALK | anaplastic lymphoma kinase | 未分化リンパ腫キナーゼ |
| BSC | best supportive care | 緩和治療,ベストサポーティブケア |
| ECOG | eastern cooperative oncology group | 米国東海岸癌臨床試験グループ |
| EGFR | epidermal growth factor receptor | 上皮成長因子受容体 |
| mPFS | median PFS | 無増悪生存期間中央値 |
| MST | median survival time | 生存期間中央値 |
| ORR | objective response rate | 客観的奏効率 |
| OS | overall survival | 全生存期間 |
| PFS | progression free survival | 無増悪生存期間 |
| PS | performance status | 一般状態 |
| QOL | quality of life | 生活の質 |
| TKI | tyrosine kinase inhibitor | チロシンキナーゼ阻害剤 |
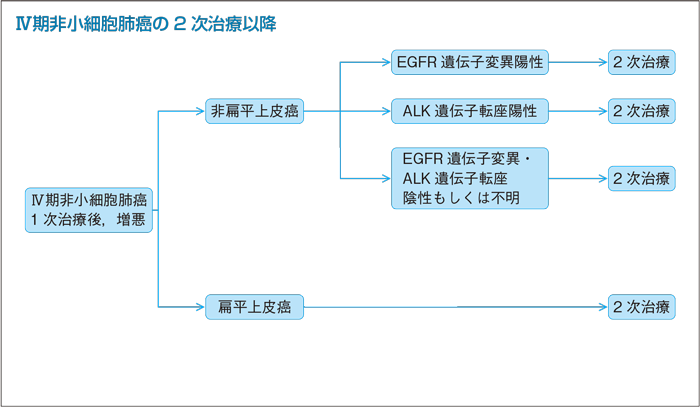
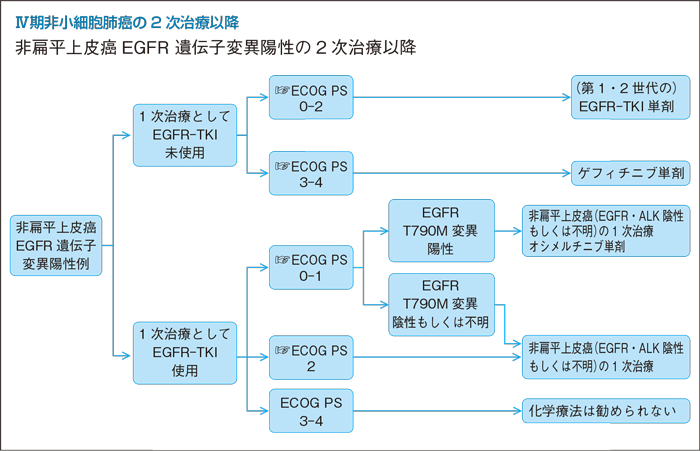
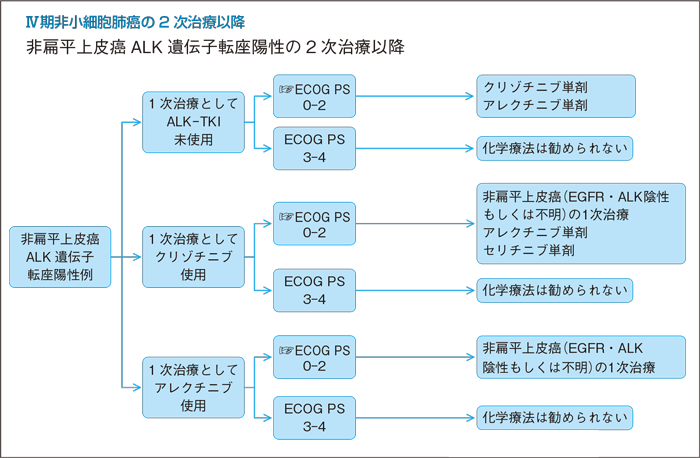
1次治療としてEGFR-TKI未使用例の2次治療以降:PS 0-2
- 推 奨
- (第1・2世代の)EGFR-TKI単剤を行うよう勧められる。(グレードA)
EGFR遺伝子変異陽性の進行非小細胞肺癌を対象にした(第1・2世代の)EGFR-TKI単剤(=ゲフィチニブ,エルロチニブ,アファチニブ)とプラチナ製剤併用療法の比較第Ⅲ相試験が行われ,すべての試験において一貫してEGFR-TKI単剤のプラチナ製剤併用療法に対するPFSの有意な延長が報告されている1)~6)。一方で,上述の試験においてEGFR-TKI単剤のプラチナ製剤併用療法に対するOSの差は示されていない7)~8)ことから, 2次治療にEGFR-TKIを用いれば1次治療にEGFR-TKIを用いた場合とほぼ同様のOSとなる可能性を示している。Rosellらの大規模研究でも1次から3次治療のエルロチニブ単剤のPFSに有意差を認めないことを報告している9)。
EGFR遺伝子変異陽性例に対するEGFR-TKI単剤の最適な投与順序に関しては,現時点で明確な結論はないが, EGFR遺伝子変異陽性患者に対してはEGFR-TKI単剤による治療を逸しないことが推奨される。
1次治療としてEGFR-TKI未使用例の2次治療以降:PS 3-4
- 推 奨
- ゲフィチニブ単剤を行うことを考慮してもよい。(グレードC1)
PS 3-4に関しては細胞障害性抗癌剤治療の適応がなく,これまで症状緩和を施行してきた。しかし,1次治療ではあるが日本人を対象にEGFR遺伝子変異のあるPS 3-4が大多数を占める予後不良群にゲフィチニブ単剤投与を行った第Ⅱ相試験において,79%の患者にPSの改善を認め,ORR 66%,OS 17.8カ月,PFS 6.5カ月と報告されている10)。
一方で,EGFR-TKIであるゲフィチニブ による間質性肺障害(ILD)のリスクが報告され,そのリスクファクターおよび発症後の予後不良因子について検討され報告され,PS不良は,EGFR-TKIによるILD発症の危険因子として知られている11)12)。
1次治療としてEGFR-TKI使用の2次治療以降:PS 0-1
- 推 奨
- a.進行期非小細胞肺癌の初回治療:PS 0-1で推奨されるレジメンを行うよう勧められる。(グレードB)
- b.EGFR T790M変異陽性ではオシメルチニブ単剤を行うよう勧められる。(グレードB)
- a.複数の1次治療の第Ⅲ相試験においてEGFR-TKI単剤はプラチナ併用療法に対して有意なOSの延長がなかった。このことは大半の症例で後治療でのクロスオーバーがなされたことが影響していると考えられている。EGFR-TKI後の治療においての最適なクロスオーバーの化学療法の詳細な検討がなされていない現状では,EGFR遺伝子変異陰性,ALK融合遺伝子陰性例での1次治療に準じて治療を行う。
- b.オシメルチニブは活性型EGFR遺伝子変異と耐性変異であるEGFR T790M変異の両方を阻害する第3世代EGFR-TKIであり,EGFR-TKIを含む治療後に病勢進行を認めたPS 0-1のEGFR遺伝子変異陽性進行非小細胞肺癌を対象とした第Ⅰ-Ⅱ相試験において,EGFR T790M変異陽性例でORR 61%,PFS 9.6カ月と良好な成績が報告された13)。また,EGFR-TKIを含む治療後に増悪し,EGFR T790M変異が陽性であったPS 0-1のEGFR遺伝子変異陽性症例を対象とした第Ⅱ相試験においても,ORR 71%,PFS 8.6カ月と良好な成績が報告されている14)。
以上はあくまで単群の試験結果でプラチナ製剤併用療法と比較したデータはないものの,少なくとも同程度の有効性は期待できると考え,推奨グレードはBとした。
1次治療としてEGFR-TKI使用の2次治療以降:PS 2
- 推 奨
- 進行期非小細胞肺癌の初回治療:PS 2で推奨されるレジメンを行うよう勧められる。(グレードB)
複数の1次治療の第Ⅲ相試験においてEGFR-TKI単剤はプラチナ併用療法に対して有意なOSの延長がなかった。このことは大半の症例で後治療でのクロスオーバーがなされたことが影響していると考えられている。EGFR-TKI後の治療においての最適なクロスオーバーの化学療法の詳細な検討がなされていない現状では,EGFR遺伝子変異陰性,ALK融合遺伝子陰性例での1次治療に準じて治療を行う。
1次治療としてALK-TKI未使用例の2次治療以降:PS 0-2
- 推 奨
- a.クリゾチニブ単剤を行うよう勧められる。(グレードA)
- b.アレクチニブ単剤を行うよう勧められる。(グレードB)
- a.レトロスペクティブ解析の結果から,ALK遺伝子転座陽性例ではクリゾチニブ投与の有無によってOSが大きく異なることが示唆されている15)。プラチナ製剤治療歴のあるALK遺伝子転座陽性例347例を対象として2次治療以降としてクリゾチニブと標準化学療法(ペメトレキセドまたはドセタキセル)を比較する第Ⅲ相試験が報告され,主要評価項目であるPFSはクリゾチニブ群が7.7カ月,標準化学療法群が3.0カ月(HR 0.49,95%CI:0.37-0.64,P<0.001)とクリゾチニブ群で有意に良好であった16)。
1次治療としてクリゾチニブ使用例の2次治療以降:PS 0-2
- 推 奨
- a.進行期非小細胞肺癌の初回治療:PS 0-2で推奨されるレジメンを行うよう勧められる。(グレードB)
- b.1次治療にクリゾチニブを使用した症例にはアレクチニブ単剤を行うよう勧められる。(グレードB)
- c.1次治療にクリゾチニブを使用した症例にはセリチニブ単剤を行うよう勧められる。(グレードB)
- a.1次治療としてALK遺伝子転座陽性の進行非小細胞肺癌を対象にしたクリゾチニブとプラチナ製剤併用療法の比較第Ⅲ相試験19)におけるOSは十分な観察期間が得られていないが,現時点では差がなく,クロスオーバーされていることが原因と考えられていること,現時点で報告されている耐性機序は化学療法と異なることより,1次治療に準じて治療を行う。
- b.クリゾチニブ耐性後のALK遺伝子転座陽性進行非小細胞肺癌を対象とし,アレクチニブを投与するⅠ-Ⅱ相試験ならびに第Ⅱ相試験が海外で行われ,ORR 48-50%,PFS 8.1-8.9カ月の良好な成績が報告されている20~22)。少数例の検討ではあるが,日本で行われたクリゾチニブ既治療の23例に対してアレクチニブを投与した試験では,ORR 65%,PFSは12.9カ月であった23)。プラチナ製剤併用療法と比較したデータはないものの,少なくとも同程度の有効性は期待できると考え,推奨グレードはBとした。
- c.ALK遺伝子転座陽性進行非小細胞肺癌を対象としセリチニブを投与する第Ⅰ相試験が行われ,expansion phaseでのサブグループ解析において,クリゾチニブ既治療の80例でORR 56%,PFS 6.9カ月の成績が報告された24)。主な毒性は悪心(82%),下痢(75%),嘔吐(65%),倦怠感(47%),肝機能障害(35%)であった。また,クリゾチニブならびにプラチナ併用療法後に増悪したALK遺伝子転座陽性例を対象とした単アームの第Ⅱ相試験において,ORR 38.6%,PFS 5.7カ月の成績が報告されている25)。本邦で行われた第Ⅰ相試験においては,クリゾチニブ既治療の9例中5例でPRの効果が得られた26)。
アレクチニブ同様,プラチナ製剤併用療法と比較したデータはないものの,少なくとも同程度の有効性は期待できると考え,推奨グレードはBとした。
1次治療としてアレクチニブ使用例の2次治療以降:PS 0-2
- 推 奨
- 進行期非小細胞肺癌の初回治療で推奨されるレジメンを行うよう勧められる。(グレードB)
現時点では,クリゾチニブのようにプラチナ製剤と比較する第Ⅲ相試験や,クリゾチニブとの比較試験の結果も出ていないが,今までのEGFR-TKI,ALK-TKIの蓄積されたデータも参考とし,TKI使用後には進行非小細胞肺癌(非扁平上皮癌,EGFR遺伝子変異,ALK遺伝子転座陰性もしくは不明)の1次治療に準じて治療を行う。
アレクチニブ使用例に対するクリゾチニブ使用については前向き試験での検討はなされていない。
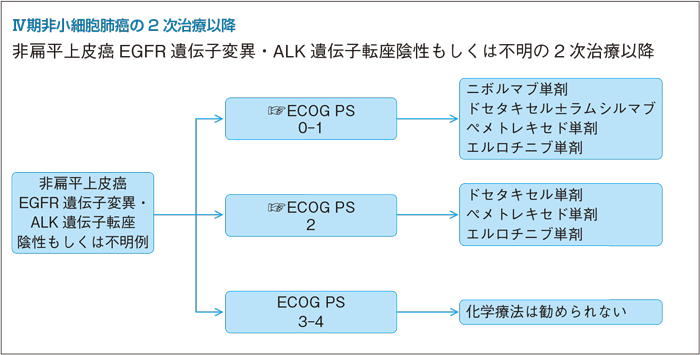
2次治療以降:PS 0-1
- 推 奨
- a.ニボルマブ単剤を行うよう勧められる。(グレードB)
- b.ラムシルマブは適応と考えられる症例においてドセタキセルに追加するよう勧められる。(グレードB)
- c.ドセタキセル単剤を行うよう勧められる。(グレードB)
- d.ペメトレキセド単剤を行うよう勧められる。(グレードB)
- e.エルロチニブ単剤を行うことを考慮してもよい。(グレードC1)
- a.プラチナ併用療法の治療歴を有する進行非扁平上皮非小細胞肺癌の2次治療として,ニボルマブ単剤とドセタキセル単剤を比較する第Ⅲ相試験が行われ,主要評価項目であるOSはニボルマブ群で有意な延長を認め(12.2カ月vs 9.4カ月,HR 0.73,P =0.002),1年生存率もニボルマブ群で良好であった(51% vs 39%)。ORRはニボルマブ群で有意に良好であったが(19% vs 12%,P =0.02),PFSはニボルマブ群で2.3カ月,ドセタキセル群で4.2カ月(HR 0.92,P =0.39)と両群に差を認めなかった。この試験におけるOS,PFSのカプランマイヤー曲線は,前半にニボルマブが下回り,6カ月以降からニボルマブが上回るという結果であった。奏効例では長期にわたる効果が期待できるなどの免疫チェックポイント阻害剤の薬剤の特性を加味する必要はあるが,非扁平上皮癌においてはニボルマブあるいはドセタキセルに対する治療反応性の異なる集団が一定の割合で存在することが示唆される。
毒性に関しては,主な毒性としてニボルマブ群で倦怠感,吐き気,食欲低下,ドセタキセル群で好中球減少,倦怠感,脱毛などであり,Grade 3以上の毒性はニボルマブ群で有意に少なかった(10% vs 54%)。一方,ニボルマブ群で肺臓炎,甲状腺機能障害,大腸炎,肝機能障害,皮疹,Ⅰ型糖尿病などの免疫関連の毒性が報告されており,免疫関連の毒性管理には注意が必要である27)。
また,本邦において再発非小細胞肺癌を対象としたニボルマブ単剤の第Ⅱ相試験が行われ,非扁平上皮癌でORR 19.7%,PFS 2.8カ月の成績が報告された。主な毒性は発熱,倦怠感,食欲低下,発疹などであり,Grade 3以上の毒性は16.2%と忍容性は良好であったが,間質性肺合併症(間質性肺炎+肺障害)が7.2%(Grade 3以上が3.6%)に認められた28)。
以上より,ニボルマブ単剤は大規模な比較第Ⅲ相試験において全体として主要評価項目であるOSで有意にドセタキセルを上回り忍容性も良好であることから行うよう勧められるが,現時点で扁平上皮癌と同様の推奨グレードとするにはデータが十分ではないと考えられ推奨グレードはBとした。
- b.プラチナ併用療法後に増悪した進行非小細胞肺癌症例を対象とし,ラムシルマブ+ドセタキセル併用療法とドセタキセル単剤療法を比較する第Ⅲ相試験が行われ,主要評価項目であるOSは,ラムシルマブ併用群で有意な延長を認めた(10.5カ月vs 9.1カ月,HR 0.86,P =0.023)。また,ラムシルマブ併用群において,PFS(4.5カ月vs. 3.0カ月,HR 0.76,P <0.0001),ORR(23% vs 14%,P <0.0001)も有意に良好であった。毒性に関しては,ラムシルマブ併用群でGrade 3/4の好中球減少,発熱性好中球減少,全Gradeの血小板減少,口内炎がより高頻度であったが,Grade 3以上の高血圧は6%で出血性イベントの多くはGrade 1/2であった29)。
また,本邦においてラムシルマブ+ドセタキセル併用療法とドセタキセル単剤療法のランダム化比較第Ⅱ相試験が行われ,ラムシルマブ併用群においてPFS(5.22カ月vs 4.21カ月,HR 0.83), OS(15.15カ月vs 13.93カ月,HR 0.77),ORR(28.9% vs 18.5%)ともに良好な結果が示された。毒性に関しては,ラムシルマブ併用群において発熱性好中球減少の頻度が高く(34% vs 19%),低アルブミン血症,血小板減少,口内炎,鼻出血,蛋白尿などもドセタキセル単剤よりも高頻度であったが,ほとんどはGrade 1/2であった30)。
ラムシルマブにおいてもベバシズマブと同様に出血リスクには注意が必要であり,投与に際してはその適応を十分検討する必要がある。
以上より,ラムシルマブは適応と考えられる症例においてドセタキセルに追加するよう勧められる。効果と発熱性好中球減少をはじめとする有害事象のバランスを考慮し,推奨グレードはBとした。
- c.プラチナ製剤を含む化学療法無効または奏効後に再発した非小細胞肺癌患者を対象としたドセタキセル単剤の第Ⅲ相試験が2つ報告されている。1つはドセタキセル(100mg/m2 or 75mg/m2)vsビノレルビンorイホスファミドの比較試験でMSTでは有意差を認めないもののドセタキセル75mg/m2群でコントロール群と比較してORR,26週PFS率,1年生存率の有意な改善を認めた31)。また,ドセタキセル(100mg/m2 or 75mg/m2)とBSCの比較ではMST,1年生存率は,ドセタキセル75mg/m2,BSC群でそれぞれ7.5カ月と37%,4.6カ月と19%でドセタキセル群で有意に優れ(P=0.010,P=0.003),QOLの改善も認められた32)。いずれの試験においても,ドセタキセル75mg/m2群が最も治療成績が優れており,プラチナ製剤を含む治療後の不応ないし再発例に対する非小細胞癌の化学療法としてはドセタキセル75mg/m2の有用性が確立された。本邦における承認用量は60mg/m2であるが,本邦で行われたこの用量における第Ⅱ相試験でORR 18.2%,MST 7.8カ月と上記2つの第Ⅲ相試験のドセタキセル75mg/m2と同等の効果を有する結果を報告した33)。
これらの結果より,プラチナ製剤を含む併用化学療法を使用した患者にはドセタキセル単剤の投与を行うよう勧められる。従来ドセタキセル単剤の推奨グレードはAであったが,今回2つの第Ⅲ相試験においてドセタキセル単剤はニボルマブ単剤あるいはドセタキセル+ラムシルマブ療法にOSで有意に劣っていたことから,今回推奨グレードはBとした。
- d.2004年に再発非小細胞肺癌の2次治療におけるペメトレキセド500mg/m2(3週毎)とドセタキセル75mg/m2(3週毎)のランダム化比較第Ⅲ相試験が報告された。治療効果は,ORR,MSTがPEM群で9.1%,8.3カ月,ドセタキセル単剤群で8.8%,7.9カ月であり主要評価項目であるMSTにて同等の効果が報告された。毒性に関しては,Grade 3/4好中球減少,発熱性好中球減少,全Gradeの脱毛の発現率がドセタキセル単剤群に有意に高かった34)。
同試験を組織学的にレトロスペクティブに解析した結果,MSTは,非扁平上皮癌でそれぞれ9.3カ月と8.0カ月でありHRは0.78(95%CI:0.61–1.00, P=0.047)であるのに対し,扁平上皮癌でそれぞれ6.2カ月と7.4カ月でありHRは1.56(95%CI:1.08–2.26, P=0.018)であり,扁平上皮癌で有意差をもってドセタキセル単剤群で良好であった。また,mPFSにおいても,非扁平上皮癌でそれぞれ3.1カ月と3.0カ月でHRは0.82(95%CI:0.66–1.02, P=0.076)と有意差を認めないものの,扁平上皮癌でそれぞれ2.3カ月と2.7カ月でHRは1.40(95%CI:1.01–1.96, P=0.046)であり有意差をもってドセタキセル単剤群が良好であったと報告された35) 。一方本邦では,既治療非小細胞肺癌を対象にペメトレキセド500mg/m2(3週毎)と1,000mg/m2(3週毎)のランダム化比較第Ⅱ相試験が行われ,用量による有意な効果と毒性の差を認めなかった36)。さらに,既治療非小細胞肺癌を対象にペメトレキセド500mg/m2(3週毎)と900mg/m2(3週毎)のランダム化比較第Ⅲ相試験が行われ,ORR,MST,PFSは,500mg/m2群で7.1%,6.7カ月,2.6カ月,900mg/m2群で4.3%,6.9カ月,2.8カ月と統計学的に有意差を認めず,Grade 3/4の毒性は両群とも5%未満で900mg/m2群にて毒性の頻度が高い傾向にあったと報告された37)。
これらの結果より,再発非小細胞肺癌(非扁平上皮癌)患者にペメトレキセド単剤の投与を行うよう勧められる。従来ペメトレキセド単剤の推奨グレードはAであったが,ドセタキセル単剤と同様の理由で今回推奨グレードはBとした。
- e.PS 0-3の2次治療以降の再発非小細胞肺癌患者731人をエルロチニブ単剤群とプラセボ群に2:1に割り付けたランダム化第Ⅲ相比較試験では,ORRがそれぞれ8.9% と1%(P <0.001),mPFSがそれぞれ2.2カ月と1.8カ月(P <0.001),主要評価項目であるMSTが6.7カ月と4.7カ月(P <0.001)でいずれもエルロチニブ単剤群が有意に優れていた。また,臨床因子のサブグループ解析で非喫煙者の延命効果が際立っていたが,男性・扁平上皮癌・喫煙者を含むすべてのサブグループでほぼ一定の延命効果が得られた38)。
PS 0-3の2次治療以降の再発非小細胞肺癌患者60人の日本人を対象とした第Ⅱ相試験では,ORRが28.3%,病勢コントロール率が50.0%,mPFSが77日,MSTが14.72カ月と報告された。Logistic regression analysisを用いたORRの多変量解析では,非喫煙者と喫煙者で(OR:0.06[95%CI:0.02–0.28, P <0.001])有意差をもって非喫煙者にORRが良好であった。また,Cox proportional hazards regression analysisを用いたOSの多変量解析では非喫煙者と喫煙者(HR:2.20[95%CI:1.06–4.56, P =0.035])とPS(0か1以上)(HR:2.59[95%CI:1.25–5.37, P =0.011])で非喫煙者とPS 0で有意差をもってOSが良好であると報告された39)。
また,プラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,OSはドセタキセル群が8.2カ月に対して,エルロチニブ群が5.4カ月(HR:0.73, 95%CI:0.53-1.00, P =0.05)とドセタキセル群が有意に良好であった40)。また,主要評価項目をPFSとして日本国内においてプラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,サブセット解析ではあるがエルロチニブ群のmPFSが1.3カ月に対してドセタキセル群で2.9カ月(HR:1.452, 95%CI:1.090-1.939, P =0.01)とドセタキセル群が良好であった41)。この結果より,EGFR遺伝子変異野生型の2次治療において少なくともドセタキセルの前にエルロチニブを使用する化学的根拠は乏しい。
一方で,EGFR-TKIであるゲフィチニブ による間質性肺障害(ILD)のリスクが報告され,そのリスクファクターおよび発症後の予後不良因子について検討され報告されている11)12)。
これらの結果より,EGFR mutation陰性もしくは不明のPS 0-2の2次治療にエルロチニブ単剤の投与を行うことは妥当である。しかし,ILDの発症リスクや予後を含め慎重に症例を選択する必要がある。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
2次治療以降:PS 2
- 推 奨
- a.ドセタキセル単剤の投与を行うよう勧められる。(グレードA)
- b.ペメトレキセド単剤の投与を行うよう勧められる。(グレードA)
- c.エルロチニブ単剤の投与を行うことを考慮してもよい。(グレードC1)
- a.プラチナ製剤を含む化学療法無効または奏効後に再発した非小細胞肺癌患者を対象としたドセタキセル単剤の第Ⅲ相試験が2つ報告されている。1つはドセタキセル(100mg/m2 or 75mg/m2)vsビノレルビンorイホスファミドの比較試験でMSTでは有意差を認めないもののドセタキセル75mg/m2群でコントロール群と比較してORR,26週PFS率,1年生存率の有意な改善を認めた31)。また,ドセタキセル(100mg/m2 or 75mg/m2)とBSCの比較ではMST,1年生存率は,ドセタキセル75mg/m2,BSC群でそれぞれ7.5カ月と37%,4.6カ月と19%でドセタキセル群で有意に優れ(P=0.010,P=0.003),QOLの改善も認められた32)。いずれの試験においても,ドセタキセル75mg/m2群が最も治療成績が優れており,プラチナ製剤を含む治療後の不応ないし再発例に対する非小細胞癌の化学療法としてはドセタキセル75mg/m2の有用性が確立された。本邦における承認用量は60mg/m2であるが,本邦で行われたこの用量における第Ⅱ相試験でORR 18.2%,MST 7.8カ月と上記2つの第Ⅲ相試験のドセタキセル75mg/m2と同等の効果を有する結果を報告した33)。
これらの結果より,プラチナ製剤を含む併用化学療法を使用した患者にはドセタキセル単剤の投与を行うよう勧められる。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- b.2004年に再発非小細胞肺癌の2次治療におけるペメトレキセド500mg/m2(3週毎)とドセタキセル75mg/m2(3週毎)のランダム化比較第Ⅲ相試験が報告された。治療効果は,ORR,MSTがPEM群で9.1%,8.3カ月,ドセタキセル単剤群で8.8%,7.9カ月であり主要評価項目であるMSTにて同等の効果が報告された。毒性に関しては,Grade 3/4好中球減少,発熱性好中球減少,全Gradeの脱毛の発現率がドセタキセル単剤群に有意に高かった34)。
同試験を組織学的にレトロスペクティブに解析した結果,OSは,非扁平上皮癌でそれぞれ9.3カ月と8.0カ月でありHRは0.78(95%CI : 0.61-1.00, P=0.047)であるのに対し,扁平上皮癌でそれぞれ6.2カ月と7.4カ月でありHRは1.56(95%CI : 1.08-2.26, P=0.018)であり,扁平上皮癌で有意差をもってドセタキセル単剤群で良好であった。また,mPFSにおいても,非扁平上皮癌でそれぞれ3.1カ月と3.0カ月でHRは0.82(95%CI : 0.66-1.02, P=0.076)と有意差を認めないものの,扁平上皮癌でそれぞれ2.3カ月と2.7カ月でHRは1.40(95%CI : 1.01-1.96, P=0.046)であり有意差をもってドセタキセル単剤群が良好であったと報告された35)。一方本邦では,既治療非小細胞肺癌を対象にペメトレキセド500mg/m2(3週毎)と1,000mg/m2(3週毎)のランダム化比較第Ⅱ相試験が行われ,用量による有意な効果と毒性の差を認めなかった36)。さらに,既治療非小細胞肺癌を対象にペメトレキセド500mg/m2(3週毎)と900mg/m2(3週毎)のランダム化比較第Ⅲ相試験が行われ,ORR,MST,mPFSは,500mg/m2群で7.1%,6.7カ月,2.6カ月,900mg/m2群で4.3%,6.9カ月,2.8カ月と統計学的に有意差を認めず,Grade 3/4の毒性は両群とも5%未満で900mg/m2群にて毒性の頻度が高い傾向にあったと報告された37)。
これらの結果より,再発非小細胞肺癌(非扁平上皮癌)患者にペメトレキセド単剤の投与を行うよう勧められる。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- c.PS 0-3の2次治療以降の再発非小細胞肺癌患者731人をエルロチニブ単剤群とプラセボ群に2:1に割り付けたランダム化第Ⅲ相比較試験では,ORRがそれぞれ8.9%と1%(P<0.001),mPFSがそれぞれ2.2カ月と1.8カ月(P<0.001),主要評価項目であるOSが6.7カ月と4.7カ月(P<0.001)でいずれもエルロチニブ単剤群が有意に優れていた。また,臨床因子のサブグループ解析で非喫煙者の延命効果が際立っていたが,男性・扁平上皮癌・喫煙者を含むすべてのサブグループでほぼ一定の延命効果が得られた38)。
PS 0-3の2次治療以降の再発非小細胞肺癌患者60人の日本人を対象とした第Ⅱ相試験では,ORRが28.3%,病勢コントロール率が50.0%,mPFSが77日,MSTが14.72カ月と報告された。Logistic regression analysisを用いたORRの多変量解析では,非喫煙者と喫煙者で(OR:0.06[95%CI : 0.02-0.28, P<0.001])有意差をもって非喫煙者にORRが良好であった。また,Cox proportional hazards regression analysisを用いたOSの多変量解析では非喫煙者と喫煙者(HR:2.20[95%CI : 1.06-4.56, P=0.035])とPS(0か1以上)(HR:2.59[95%CI : 1.25-5.37, P=0.011])で非喫煙者とPS 0で有意差をもってOSが良好であると報告された39)。
また,プラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,OSはドセタキセル群が8.2カ月に対して,エルロチニブ群が5.4カ月(HR:0.73, 95%CI : 0.53-1.00, P=0.05)とドセタキセル群が有意に良好であった40)。また,主要評価項目をPFSとして日本国内においてプラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,サブセット解析ではあるがエルロチニブ群のmPFSが1.3カ月に対してドセタキセル群で2.9カ月(HR 1.452, 95%CI : 1.090-1.939, P=0.01)とドセタキセル群が良好であった41)。この結果より,EGFR遺伝子変異野生型の2次治療において少なくともドセタキセルの前にエルロチニブを使用する科学的根拠は乏しい。
一方で,EGFR-TKIであるゲフィチニブ による間質性肺障害(ILD)のリスクが報告され,そのリスクファクターおよび発症後の予後不良因子について検討され報告されている11)12)。
これらの結果より,EGFR mutation陰性もしくは不明のPS 0-2の2次治療にエルロチニブ単剤の投与を行うことは妥当である。しかし,ILDの発症リスクや予後を含め慎重に症例を選択する必要がある。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
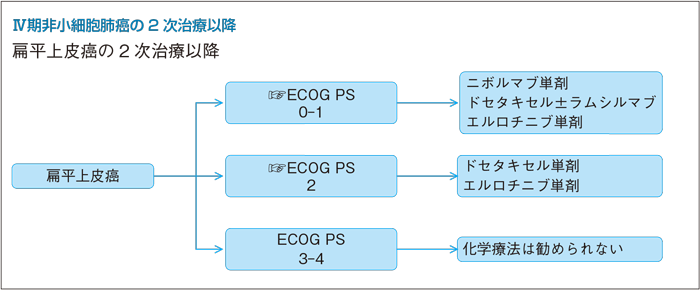
- 推 奨
- a.ニボルマブ単剤を行うよう勧められる。(グレードA)
- b.ラムシルマブは適応と考えられる症例においてドセタキセルに追加するよう勧められる。(グレードB)
- c.ドセタキセル単剤を行うよう勧められる。(グレードB)
- d.エルロチニブ単剤を行うことを考慮してもよい。(グレードC1)
- a.プラチナ併用療法の治療歴を有する進行扁平上皮非小細胞肺癌の2次治療として,ニボルマブ単剤とドセタキセル単剤を比較する第Ⅲ相試験が行われ,主要評価項目であるOSはニボルマブ群で有意な延長を認め(9.2カ月vs 6.0カ月,HR 0.59,P <0.001),1年生存率もニボルマブ群で良好であった(42% vs 24%)。また,ニボルマブ群においてPFS(3.5カ月vs 2.8カ月,HR 0.62,P <0.001),ORR(20% vs 9%,P =0.008)も有意に良好であった。主な毒性は,ニボルマブ群で倦怠感や食欲低下,ドセタキセル群で好中球減少,倦怠感,脱毛などであり,Grade 3以上の毒性はニボルマブ群で有意に少なかった(7% vs 55%)。一方,ニボルマブ群で肺臓炎,甲状腺機能障害,大腸炎,肝機能障害,皮疹,Ⅰ型糖尿病などの免疫関連の毒性が報告されており,免疫関連の毒性管理には注意が必要である42)。
また,本邦において再発非小細胞肺癌を対象としたニボルマブ単剤の第Ⅱ相試験が行われ,扁平上皮癌でORR 25.7%,mPFS 4.2カ月の成績が報告された。主な毒性は発熱,倦怠感,食欲低下,発疹などであり,Grade 3以上の毒性は16.2%と忍容性は良好であったが,間質性肺合併症(間質性肺炎+肺障害)が7.2%(Grade 3以上が3.6%)に認められた28)。
以上より,ニボルマブ単剤の投与を行うよう勧められ,比較第Ⅲ相試験においてドセタキセル単剤よりHR 0.59という差でOSを上回っており,忍容性も良好であることから臨床的有用性が高いと考えられ,推奨グレードはAとした。
- b.プラチナ併用療法後に増悪した進行非小細胞肺癌症例を対象とし,ラムシルマブ+ドセタキセル併用療法とドセタキセル単剤療法を比較する第Ⅲ相試験が行われ,主要評価項目であるOSは,ラムシルマブ併用群で有意な延長を認めた(MST 10.5カ月vs 9.1カ月,HR 0.86,P =0.023)。また,ラムシルマブ併用群において,PFS(mPFS 4.5カ月vs. 3.0カ月, HR 0.76,P <0.0001),ORR(23% vs 14%,P<0.0001)も有意に良好であった。毒性に関しては,ラムシルマブ併用群でGrade 3/4の好中球減少,発熱性好中球減少,全Gradeの血小板減少,口内炎がより高頻度であったが,Grade 3以上の高血圧は6%で出血性イベントの多くはGrade 1/2であった29)。
また,本邦においてラムシルマブ+ドセタキセル併用療法とドセタキセル単剤療法のランダム化比較第Ⅱ相試験が行われ,ラムシルマブ併用群においてPFS(mPFS 5.22カ月vs 4.21カ月,HR 0.83),OS(MST 15.15カ月vs 13.93カ月,HR 0.77),ORR(28.9% vs 18.5%)ともに良好な結果が示された。毒性に関しては,ラムシルマブ併用群において発熱性好中球減少の頻度が高く(34% vs 19%),低アルブミン血症,血小板減少,口内炎,鼻出血,蛋白尿などもドセタキセル単剤よりも高頻度であったが,ほとんどはGrade 1/2であった30)。
ラムシルマブにおいてもベバシズマブと同様に出血リスクには注意が必要であり,投与に際してはその適応を十分検討する必要がある。
以上より,ラムシルマブは適応と考えられる症例においてドセタキセルに追加するよう勧められる。効果と発熱性好中球減少をはじめとする有害事象のバランスを考慮し,推奨グレードはBとした。
- c.プラチナ製剤を含む化学療法無効または奏効後に再発した非小細胞肺癌患者を対象としたドセタキセル単剤の第Ⅲ相試験が2つ報告されている。1つはドセタキセル(100mg/m2 or 75mg/m2) vsビノレルビンorイホスファミドの比較試験でMSTでは有意差を認めないもののドセタキセル75mg/m2群でコントロール群と比較してORR,26週PFS率,1年生存率の有意な改善を認めた31)。また,ドセタキセル(100mg/m2 or 75mg/m2)とBSCの比較ではMST,1年生存率は,ドセタキセル75mg/m2,BSC群でそれぞれ7.5カ月と37%,4.6カ月と19%でドセタキセル群で有意に優れ(P =0.010,P =0.003),QOLの改善も認められた32)。いずれの試験においても,ドセタキセル75mg/m2群が最も治療成績が優れており,プラチナ製剤を含む治療後の不応ないし再発例に対する非小細胞癌の化学療法としてはドセタキセル75mg/m2の有用性が確立された。本邦における承認用量は60mg/m2であるが,本邦で行われたこの用量における第Ⅱ相試験でORR 18.2%,MST 7.8カ月と上記2つの第Ⅲ相試験のドセタキセル75mg/m2と同等の効果を有する結果を報告した33)。
これらの結果より,プラチナ製剤を含む併用化学療法を使用した患者にはドセタキセル単剤の投与を行うよう勧められる。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- d.PS 0-3の2次治療以降の再発非小細胞肺癌患者731人をエルロチニブ単剤群とプラセボ群に2:1に割り付けたランダム化第Ⅲ相比較試験では,ORRがそれぞれ8.9% と1%(P<0.001),mPFSがそれぞれ2.2カ月と1.8カ月(P <0.001),主要評価項目であるOSではMSTが6.7カ月と4.7カ月(P<0.001)でいずれもエルロチニブ単剤群が有意に優れていた。また,臨床因子のサブグループ解析で非喫煙者の延命効果が際立っていたが,男性・扁平上皮癌・喫煙者を含むすべてのサブグループでほぼ一定の延命効果が得られた38)。
PS 0-3の2次治療以降の再発非小細胞肺癌患者60人の日本人を対象とした第Ⅱ相試験では,ORRが28.3%,病勢コントロール率が50.0%,PFSが77日,MSTが14.72カ月と報告された。Logistic regression analysisを用いたORRの多変量解析では,非喫煙者と喫煙者で(OR:0.06[95%CI:0.02–0.28, P<0.001])有意差をもって非喫煙者にORRが良好であった。また,Cox proportional hazards regression analysisを用いたOSの多変量解析では非喫煙者と喫煙者(HR:2.20[95%CI:1.06–4.56, P=0.035])とPS(0か1以上)(HR:2.59[95%CI:1.25–5.37, P=0.011])で非喫煙者とPS 0で有意差をもってOSが良好であると報告された39)。また,プラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,OSはドセタキセル群がMST 8.2カ月に対して,エルロチニブ群がMST 5.4カ月(HR:0.73, 95%CI:0.53-1.00, P =0.05)とドセタキセル群が有意に良好であった40)。また,主要評価項目をPFSとして日本国内においてプラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,サブセット解析ではあるがエルロチニブ群のPFSがmPFS 1.3カ月に対してドセタキセル群でmPFS 2.9カ月(HR:1.452,95%CI:1.090-1.939, P=0.01)とドセタキセル群が良好であった41)。この結果より,EGFR遺伝子変異野生型の2次治療において少なくともドセタキセルの前にエルロチニブを使用する化学的根拠は乏しい。
一方で,EGFR-TKIであるゲフィチニブ による間質性肺障害(ILD)のリスクが報告され,そのリスクファクターおよび発症後の予後不良因子について検討され報告されている11)12)。
これらの結果より,EGFR mutation陰性もしくは不明のPS 0-2の2次治療にエルロチニブ単剤の投与を行うことは妥当である。しかし,ILDの発症リスクや予後を含め慎重に症例を選択する必要がある。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- 推 奨
- a.ドセタキセル単剤を行うよう勧められる。(グレードA)
- b.エルロチニブ単剤を行うことを考慮してもよい。(グレードC1)
- a.プラチナ製剤を含む化学療法無効または奏効後に再発した非小細胞肺癌患者を対象としたドセタキセル単剤の第Ⅲ相試験が2つ報告されている。1つはドセタキセル(100mg/m2 or 75mg/m2) vs ビノレルビン or イホスファミドの比較試験でMSTでは有意差を認めないもののドセタキセル75mg/m2群でコントロール群と比較してORR,26週PFS率,1年生存率の有意な改善を認めた31)。また,ドセタキセル(100mg/m2 or 75mg/m2)とBSCとの比較ではMST,1年生存率は,ドセタキセル75mg/m2,BSC群でそれぞれ7.5カ月と37%,4.6カ月と19%でドセタキセル群で有意に優れ(P=0.010,P=0.003),QOLの改善も認められた32)。いずれの試験においても,ドセタキセル75mg/m2群が最も治療成績が優れており,プラチナ製剤を含む治療後の不応ないし再発例に対する非小細胞癌の化学療法としてはドセタキセル75mg/m2の有用性が確立された。本邦における承認用量は60mg/m2であるが,本邦で行われたこの用量における第Ⅱ相試験でORR 18.2%,MST 7.8カ月と上記2つの第Ⅲ相試験のドセタキセル75mg/m2と同等の効果を有する結果を報告した33)。
これらの結果より,プラチナ製剤を含む併用化学療法を使用した患者にはドセタキセル単剤の投与を行うよう勧められる。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- b.PS 0-3の2次治療以降の再発非小細胞肺癌患者731人をエルロチニブ単剤群とプラセボ群に2:1に割り付けたランダム化第Ⅲ相比較試験では,ORRがそれぞれ8.9%と1%(P<0.001),PFSがそれぞれ2.2カ月と1.8カ月(P<0.001),主要評価項目であるOSが6.7カ月と4.7カ月(P<0.001)でいずれもエルロチニブ単剤群が有意に優れていた。また,臨床因子のサブグループ解析で非喫煙者の延命効果が際立っていたが,男性・扁平上皮癌・喫煙者を含むすべてのサブグループでほぼ一定の延命効果が得られた38)。
PS 0-3の2次治療以降の再発非小細胞肺癌患者60人の日本人を対象とした第Ⅱ相試験では,ORRが28.3%,病勢コントロール率が50.0%,mPFSが77日,MSTが14.72カ月と報告された。Logistic regression analysisを用いたORRの多変量解析では,非喫煙者と喫煙者で(OR:0.06[95%CI:0.02-0.28, P<0.001])有意差をもって非喫煙者にORRが良好であった。また,Cox proportional hazards regression analysisを用いたOSの多変量解析では非喫煙者と喫煙者(HR:2.20[95%CI : 1.06-4.56, P=0.035])とPS(0か1以上)(HR:2.59[95%CI : 1.25-5.37, P=0.011])で非喫煙者とPS 0で有意差をもってOSが良好であると報告された39)。
また,プラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,OSはドセタキセル群がMST 8.2カ月に対して,エルロチニブ群がMST 5.4カ月(HR:0.73,95% CI 0.53-1.00; P=0.05)とドセタキセル群が有意に良好であった40)。また,主要評価項目をPFSとして日本国内においてプラチナ製剤治療歴のあるEGFR遺伝子変異野生型症例を対象とし,2次治療としてドセタキセルとエルロチニブを比較する第Ⅲ相試験が報告され,サブセット解析ではあるがエルロチニブ群のPFSがmPFS 1.3カ月に対してドセタキセル群でmPFS 2.9カ月(HR:1.452,95%CI:1.090-1.939,P =0.01)とドセタキセル群が良好であった41)。この結果より,EGFR遺伝子変異野生型の2次治療において少なくともドセタキセルの前にエルロチニブを使用する化学的根拠は乏しい。
一方で,EGFR-TKIであるゲフィチニブ による間質性肺障害(ILD)のリスクが報告され,そのリスクファクターおよび発症後の予後不良因子について検討され報告されている11)12)。
これらの結果より,EGFR mutation陰性もしくは不明のPS 0-2の2次治療にエルロチニブ単剤の投与を行うことは妥当である。しかし,ILDの発症リスクや予後を含め慎重に症例を選択する必要がある。また,2次治療の臨床試験はプラチナ製剤使用症例が対象となっているため,プラチナ製剤未使用症例に対する2次治療での単剤療法のエビデンスは乏しい。
- 1) Mitsudomi T, Morita S, Yatabe Y, et al. Gefitinib versus cisplatin plus docetaxel in patients with non-small-cell lung cancer harbouring mutations of the epidermal growth factor receptor(WJTOG3405): an open label, randomised phase 3 trial. Lancet Oncol. 2010; 11(2): 121-8. (II)
- 2) Maemondo M, Inoue A, Kobayashi K, et al. Gefitinib or chemotherapy for non-small-cell lung cancer with mutated EGFR. N Engl J Med. 2010; 362(25): 2380-8. (II)
- 3) Zhou C, Wu YL, Chen G, et al. Erlotinib versus chemotherapy as first-line treatment for patients with advanced EGFR mutation-positive non-small-cell lung cancer(OPTIMAL, CTONG-0802): a multicentre, open-label, randomised, phase 3 study. Lancet Oncol. 2011; 12(8): 735-42. (II)
- 4) Rosell R, Carcereny E, Gervais R, et al. Erlotinib versus standard chemotherapy as first-line treatment for European patients with advanced EGFR mutation-positive non-small-cell lung cancer(EURTAC): a multicentre, open-label, randomised phase 3 trial. Lancet Oncol. 2012; 13(3): 239-46. (II)
- 5) Sequist LV, Yang JC, Yamamoto N, et al. Phase III study of afatinib or cisplatin plus pemetrexed in patients with metastatic lung adenocarcinoma with EGFR mutations. J Clin Oncol. 2013; 31(27): 3327-34.(II)
- 6) Wu YL, Zhou C, Hu CP, et al. Afatinib versus cisplatin plus gemcitabine for first-line treatment of Asian patients with advanced non-small-cell lung cancer harbouring EGFR mutations(LUX-Lung 6): an open-label, randomised phase 3 trial. Lancet Oncol. 2014; 15(2): 213-22. (II)
- 7) Inoue A, Kobayashi K, Maemondo M, et al. Updated overall survival results from a randomized phase III trial comparing gefitinib with carboplatin-paclitaxel for chemo-naïve non-small cell lung cancer with sensitive EGFR gene mutations(NEJ002). Ann Oncol. 2013; 24(1): 54-9. (II)
- 8) Zhou C, Wu YL, Liu X, et al. Overall survival(OS)results from OPTIMAL(CTONG0802), a phase III trial of erlotinib(E)versus carboplatin plus gemcitabine(GC)as first-line treatment for Chinese patients with EGFR mutation-positive advanced non-small cell lung cancer(NSCLC). J Clin Oncol. 30, 2012(suppl; abstr 7520). (II)
- 9)Rosell R, Moran T, Queralt C, et al. Screening for epidermal growth factor receptor mutations in lung cancer. N Engl J Med. 2009; 361(10): 958-67. (III)
- 10)Inoue A, Kobayashi K, Usui K, et al. First-line gefitinib for patients with advanced non-small-cell lung cancer harboring epidermal growth factor receptor mutations without indication for chemotherapy. J Clin Oncol. 2009; 27(9): 1394-400. (III)
- 11)Kudoh S, Kato H, Nishiwaki Y, et al. Interstitial lung disease in Japanese patients with lung cancer: a cohort and nested case-control study. Am J Respir Crit Care Med. 2008; 177(12): 1348-57. (IV)
- 12)Ando M, Okamoto I, Yamamoto N, et al. Predictive factors for interstitial lung disease, antitumor response, and survival in non-small-cell lung cancer patients treated with gefitinib. J Clin Oncol. 2006; 24(16): 2549-56.(IV)
- 13) Jänne PA, Yang JC, Kim DW, et al. AZD9291 in EGFR inhibitor-resistant non-small-cell lung cancer. N Engl J Med. 2015; 372 (18) : 1689-99.(IV)
- 14) Mitsudomi T, Tsai C, Shepherd L, et al. AZD9291 in pre-treated T790M positive advanced NSCLC : AURA 2 Phase II study. J Thorac Oncol. 2015; 10 (9) : suppl 2; MINI 16.08.(IV)
- 15) Shaw AT, Yeap BY, Solomon BJ, et al. Effect of crizotinib on overall survival in patients with advanced non-small-cell lung cancer harbouring ALK gene rearrangement: a retrospective analysis. Lancet Oncol. 2011; 12(11): 1004-12.(IV)
- 16)Shaw AT, Kim DW, Nakagawa K, et al. Crizotinib versus chemotherapy in advanced ALK-positive lung cancer. N Engl J Med. 2013; 368(25): 2385-94. (II)
- 17) Seto T, Kiura K, Nishio M, et al. CH5424802(RO5424802)for patients with ALK-rearranged advanced non-small-cell lung cancer(AF-001JP study): a single-arm, open-label, phase 1-2 study. Lancet Oncol. 2013; 14(7): 590-8.(IV)
- 18) Ohe Y, Nishio M, Kiura K, et al. A phase I/II study with a CNS-penetrant, selective ALK inhibitor alectinib in ALK-rearranged non-small cell lung cancer patients: Updates on progression free survival and safety results from AF-001JP. J Clin Oncol. 2015; 33 (suppl; abstr 8061). (IV)
- 19) Solomon BJ, Mok T, Kim DW, et al; PROFILE 1014 Investigators. First-line crizotinib versus chemotherapy in ALK-positive lung cancer. N Engl J Med. 2014; 371(23): 2167-77. (II)
- 20) Gadgeel SM, Gandhi L, Riely GJ, et al. Safety and activity of alectinib against systemic disease and brain metastases in patients with crizotinib-resistant ALK-rearranged non-small-cell lung cancer (AF-002JG): results from the dose-finding portion of a phase 1/2 study. Lancet Oncol. 2014;15(10):1119-28. (III)
- 21) Ou SHI, Ahn JS, De Petris L, et al. Efficacy and safety of the ALK inhibitor alectinib in ALK+ non-small-cell lung cancer (NSCLC) patients who have failed prior crizotinib: an open-label, single-arm, global phase 2 study (NP28673). J Clin Oncol. 2015; 33 (suppl; abstr 8008). (III)
- 22) Shaw A, West H, Socinski MA, et al. Updated Efficacy/Safety Data From the Phase 2 NP28761 Study of Alectinib in ALK+ NSCLC. J Thorac Oncol. 2015; 10(9): suppl 2; ORAL33.03. (III)
- 23) Hotta K, Hida T, Nakagawa K, et al. Updated data from JP28927 study of alectinib in ALK+ NSCLC patients with or without history of ALK inhibitor treatment. J Thorac Oncol. 2015; 10(9): suppl 2; P3.01-020.
- 24) Shaw AT, Kim DW, Mehra R, et al. Ceritinib in ALK-rearranged non-small-cell lung cancer. N Engl J Med. 2014; 370 (13) : 1189-97.(IV)
- 25) Mok T, Spigel D, Felip E, et al. ASCEND-2: A single-arm, open-label, multicenter phase II study of ceritinib in adult patients (pts) with ALK-rearranged (ALK+) non-small cell lung cancer (NSCLC) previously treated with chemotherapy and crizotinib (CRZ). J Clin Oncol. 2015; 33 (suppl; abstr 8059).(IV)
- 26) Nishio M, Murakami H, Horiike A, et al. Phase I Study of Ceritinib (LDK378) in Japanese Patients with Advanced, Anaplastic Lymphoma Kinase-Rearranged Non-Small-Cell Lung Cancer or Other Tumors. J Thorac Oncol. 2015; 10 (7) : 1058-66.(IV)
- 27) Borghaei H, Paz-Ares L, Horn L, et al. Nivolumab versus Docetaxel in Advanced Nonsquamous Non-Small-Cell Lung Cancer. N Engl J Med. 2015; 373 (17) : 1627-39.(II)
- 28) Nishio M, Hida T, Nakagawa K, et al. Phase II studies of nivolumab (anti-PD-1, BMS-936558, ONO-4538) in patients with advanced squamous (sq) or nonsquamous (non-sq) non-small cell lung cancer (NSCLC). J Clin Oncol. 2015; 33 (suppl; abstr 8027).(IV)
- 29) Garon EB, Ciuleanu TE, Arrieta O, et al. Ramucirumab plus docetaxel versus placebo plus docetaxel for second-line treatment of stage IV non-small-cell lung cancer after disease progression on platinum-based therapy (REVEL): a multicentre, double-blind, randomised phase 3 trial. Lancet. 2014; 23; 384 (9944) : 665-73.(II)
- 30) Hosomi Y, Yoh K, Kasahara K, et al. Docetaxel + ramucirumab (DR) versus docetaxel + placebo (D) as second-line treatment for advanced non-small cell lung cancer (NSCLC): A randomized, phase II, double-blind, multicenter trial in Japan. J Clin Oncol. 2015; 33 (suppl; abstr 8054).(II)
- 31)Fossella FV, DeVore R, Kerr RN, et al. Randomized phase III trial of docetaxel versus vinorelbine or ifosfamide in patients with advanced non-small-cell lung cancer previously treated with platinum-containing chemotherapy regimens. The TAX 320 Non-Small Cell Lung Cancer Study Group. J Clin Oncol. 2000; 18(12): 2354-62. (II)
- 32)Shepherd FA, Dancey J, Ramlau R, et al. Prospective randomized trial of docetaxel versus best supportive care in patients with non-small-cell lung cancer previously treated with platinum-based chemotherapy. J Clin Oncol. 2000; 18(10): 2095-103. (II)
- 33)Mukohara T, Takeda K, Miyazaki M, et al. Japanese experience with second-line chemotherapy with low-dose (60mg/M2) docetaxel in patients with advanced non-small-cell lung cancer. Cancer Chemother Pharmacol. 2001; 48(5): 356-60. (IV)
- 34)Hanna N, Shepherd FA, Fossella FV, et al. Randomized phase III trial of pemetrexed versus docetaxel in patients with non-small-cell lung cancer previously treated with chemotherapy. J Clin Oncol. 2004; 22(9): 1589-97. (II)
- 35)Scagliotti G, Hanna N, Fossella F, et al. The differential efficacy of pemetrexed according to NSCLC histology: a review of two Phase III studies. Oncologist. 2009; 14(3): 253-63. (II)
- 36)Ohe Y, Ichinose Y, Nakagawa K, et al. Efficacy and safety of two doses of pemetrexed supplemented with folic acid and vitamin B12 in previously treated patients with non-small cell lung cancer. Clin Cancer Res. 2008; 14(13): 4206-12. (II)
- 37)Cullen MH, Zatloukal P, Sörenson S, et al. A randomized phase III trial comparing standard and high-dose pemetrexed as second-line treatment in patients with locally advanced or metastatic non-small-cell lung cancer. Ann Oncol. 2008; 19(5): 939-45. (IV)
- 38)Shepherd FA, Rodrigues Pereira J, Ciuleanu T, et al. Erlotinib in previously treated non-small-cell lung cancer. N Engl J Med. 2005; 353(2): 123-32. (II)
- 39)Kubota K, Nishiwaki Y, Tamura T, et al. Efficacy and safety of erlotinib monotherapy for Japanese patients with advanced non-small cell lung cancer: a phase II study. J Thorac Oncol. 2008; 3(12): 1439-45. (III)
- 40) Garassino MC, Martelli O, Broggini M, et al. Erlotinib versus docetaxel as second-line treatment of patients with advanced non-small-cell lung cancer and wild-type EGFR tumours(TAILOR): a randomised controlled trial. Lancet Oncol. 2013; 14(10): 981-8.(II)
- 41) Kawaguchi T, Ando M, Asami K, et al. Randomized phase III trial of erlotinib versus docetaxel as second- or third-line therapy in patients with advanced non-small-cell lung cancer: Docetaxel and Erlotinib Lung Cancer Trial(DELTA). J Clin Oncol. 2014; 32(18): 1902-8. (II)
- 42) Brahmer J, Reckamp KL, Baas P, et al. Nivolumab versus Docetaxel in Advanced Squamous-Cell Non-Small-Cell Lung Cancer. N Engl J Med. 2015; 373 (2) : 123-35.(II)
| Nivolumab | 3mg/kg, on day1 | q2w |
| DTX | 60mg/m2, on day1 | q3w |
| Ramucirumab | 10mg/kg, on day1 | |
| DTX | 60mg/m2, day1 | q3w |
| PEM | 500mg/m2, day1 | q3w |
| ※PEMの投与に際しては下記ビタミンの補充を行う ①葉酸:投与の7日以上前から葉酸として1日1回0.5mgを連日経口投与する。なお,本剤の投与を中止または終了する場合には,本剤最終投与日から22日目まで可能な限り葉酸を投与する。 ②ビタミンB12:初回投与の少なくとも7日前に,ビタミンB12として1回1mgを筋肉内投与する。その後,本剤投与期間中および投与中止後22日目まで9週ごと(3コースごと)に1回投与する。 |
||
| Gefitinib | 250mg/日 1錠 | 1日1回 |
| Erlotinib | 150mg/日 1錠 | 1日1回 |
| Afatinib | 40mg/日 1錠 | 1日1回 |
| Osimertinib | 80mg/日 1錠 | 1日1回 |
| Crizotinib | 500mg/日 1回250mg | 1日2回 |
| Alectinib | 600mg/日 (40mg)7錠,(20mg)1錠 | 1日2回 |
| Ceritinib | 750mg/日 | 1日1回 |