3
Ⅱ.治 療
化学療法
文献検索と採択
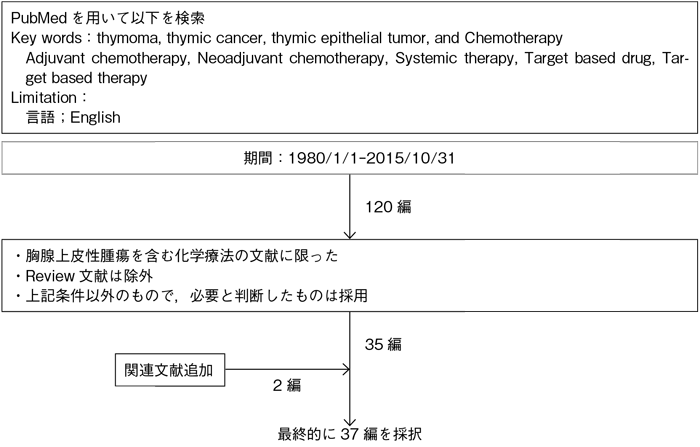
3-1.胸腺腫に対する化学治療
- 推 奨
- <初回治療>
a.臨床病期Ⅳ期(AnyTAnyNM1a, b)または再発胸腺腫に対しての化学療法は,科学的根拠は明確ではないが行うことを考慮してもよい。(グレードC1)
- <レジメン>
b.シスプラチンおよびアンスラサイクリン系抗癌剤の併用療法を,科学的根拠は明確ではないが行うことを考慮してもよい。(グレードC1)
c.アンスラサイクリン系が使用できない場合は,非アンスラサイクリン系抗癌剤の併用療法を科学的根拠は明確ではないが行うことを考慮してもよい。(グレードC1)
d.シスプラチン単剤での化学療法は行わないよう勧められる。(グレードD)
- <二次治療>
e.一次治療に不応となった胸腺腫に対しての化学療法は,行うよう勧められるだけの科学的根拠が明確ではない。(グレードC2)
エビデンス
- a.
- 臨床病期Ⅳ期(AnyTAnyNM1a, b)胸腺腫や手術後に再発し根治手術が困難な例が対象となる。
これまでに胸腺腫を対象とした化学療法の臨床試験はランダム化比較試験はなく,エビデンスレベルの低い少数例による第Ⅱ相試験やレトロスペクティブな報告がほとんどであり,化学療法を行うことが予後をどれくらい改善できるかは不明である。さらに本邦では保険適応となる抗癌剤はない。しかし胸腺腫はこれまでの報告では化学療法に対して比較的高い奏効率が報告されており,化学療法による症状緩和の効果は十分期待できることより,PS 0-2など全身状態良好な症例では化学療法は科学的根拠は明確ではないが行うことを考慮してもよいとした(グレードC1)。 - b.
- 本邦および海外で報告された胸腺腫に対する化学療法は主にアンスラサイクリン系を軸とした併用療法が多い。CDDP+アンスラサイクリン系を用いた治療としては,ADOC療法1),PAC療法2),CODE療法3),CAMP療法4)5)などがあり,奏効率は70~92%(平均75%)である。一方,アンスラサイクリン系を用いない治療法としては,PE療法,VIP療法6),CP療法7)などが報告されているが奏効率は35~52%(平均40%)であった。このようにプラチナ系およびアンスラサイクリン系併用療法と,プラチナ系および非アンスラサイクリン併用療法を比較するとアンスラサイクリン系のほうが良好な傾向がみられており,可能な症例ではCDDPとアンスラサイクリン系を含むレジメンが勧められる(グレードC1)。
- c.
- 合併症などからアンスラサイクリン系が使用できない場合は,PE療法8),VIP療法6),CP療法7)などは奏効率は35~52%(平均40%)であり,これらの非アンスラサイクリン系抗癌剤の併用療法を行うことも考慮してもよい(グレードC1)。
- d.
- 胸腺腫に対する初回治療として,CDDP単剤での抗癌剤治療9)は併用療法と比較し奏効率が低いことが報告されており,行わないよう勧められる(グレードD)。
- e.
- 既治療胸腺腫への化学療法に関してはPEM10)やIFM,オクトレオチド11)12)などが試されている。オクトレオチドについてはオクトレオチドシンチグラフィーで陽性またはカルチノイド症候群の症状があるケースも一部で有効性が報告されているため,該当する症例においては考慮してもよい。しかし,いずれも少数例の報告しかなく効果も限定的であり,現時点では推奨できるような治療はない。以上よりグレードC2とした。
3-2.胸腺癌に対する化学治療
- 推 奨
a.再発または転移のある胸腺癌に対しての化学療法は,科学的根拠は明確ではないが行うことを考慮してもよい。(グレードC1)
- <レジメン>
b.カルボプラチンとパクリタキセルの併用療法は,科学的根拠は明確ではないが行うことを考慮してもよい。(グレードC1)
c.ADOC療法は行うよう勧められるだけの科学的根拠が明確ではない。(グレードC2)
d.イマチニブは使用しないよう勧められる。(グレードD)
e.一次治療に不応となった胸腺癌に対しては,二次化学療法を行うように勧められるだけの科学的根拠が明確でない。(グレードC2)
エビデンス
- a.
- 胸腺癌に対する化学療法は胸腺腫よりもさらに症例が少なく,胸腺腫に準じたレジメンが主に用いられてきた。最近は胸腺癌に限定して行われた研究も報告されているが,これまでの報告の多くがレトロスペクティブな報告であり化学療法におけるエビデンスは乏しい。しかし化学療法の奏効率は約20~50%と一定の効果はみられており,全身状態がよければ行うことを考慮してもよい(グレードC1)。
- b.
- 胸腺腫と異なり,胸腺癌においてはアンスラサイクリン系と非アンスラサイクリン系レジメンとの間に大きな差はなくキードラッグははっきりしない。CP療法は複数の海外および本邦からの第Ⅱ相試験7)13)において奏効率36~42%と比較的良好であることが報告されており,治療選択の1つと考えられる(グレードC1)。また,カルボプラチンとペメトレキセド併用療法については本邦より第Ⅱ相試験が報告されており,奏効率30%と比較的良好な結果であるが,ペメトレキセドは扁平上皮癌には適応はないことよりレジメンには含めなかった。
- c.
- ADOC療法1)も胸腺癌において複数の奏効例の報告があることから考慮してもよい。ただCP療法と比較し毒性が強い傾向が報告されており,グレードC2とした。
- d.
- 胸腺癌ではc-KIT発現は73~86%と高頻度ではあるが,c-KIT遺伝子変異は約10%未満であり,C-KIT阻害薬であるイマチニブは臨床試験14)でも奏効を示していないため使用しないよう勧められる(グレードD)。
- e.
- 胸腺癌に対する二次化学療法については,ペメトレキセド10)やスニチニブ15)の治療効果が報告されている。ペメトレキセドは奏効率約10%,病勢制御率60%と報告された。C-KITやVEGFR,PDGFRなどマルチターゲット阻害薬であるスニチニブは第Ⅱ相試験でPR 26%(6/23),SD 65%(15/23)と比較的良好な結果が報告された。また,S-1が有効であったとの少数例での報告がある。しかし,いずれも少数例での報告であり,現時点では推奨できるような治療はない。以上より,胸腺癌に対する二次化学療法については確立された治療は存在しないことから,緩和治療のみも治療選択肢として検討しながら,全身状態など考慮して二次化学療法の適応を慎重に判断すべきでありグレードC2とした。
レジメン:胸腺腫/胸腺癌に対する化学療法
| レジメン名 | 治療薬剤 | 治療期間 |
|---|---|---|
| ADOC1) | アドリアシン40 mg/m2(day 1),シスプラチン50 mg/m2(day 1),ビンクリスチン0.6 mg/m2(day 2 or day 3),シクロホスファミド700 mg/m2(day 4) | 4週毎 |
| PAC2) | シスプラチン50 mg/m2(day 1),ドキソルビシン50 mg/m2(day 1),シクロホスファミド500 mg/m2(day 1) | 3週毎 (最大4コース) |
| VIP6) | シスプラチン20 mg/m2(day 1-4),エトポシド75 mg/m2(day 1-4),シクロホスファミド1,200 mg/m2(day 1-4) | 3週毎 (最大4コース) |
| CAMP4) | シクロホスファミド700 mg/m2(day 1),シスプラチン30 mg/m2(day 1-3),ドキソルビシン20 mg/m2(day 1-3),プレドニゾロン100 mg/日(day 1-5) | 3週毎 |
| CAMP5) | シスプラチン20 mg/m2(day 1-4),ドキソルビシン40 mg/m2(day 1),メチルプレドニゾロン1,000 mg/日(day 1-4)+500 mg/日(day 5, 6) | 3-4週毎 |
| CP7) | カルボプラチン(AUC=6),パクリタキセル200 mg/m2 | 3週毎 (最大6コース) |
| CODE3) | シスプラチン25 mg/m2(毎週),ビンクリスチン1 mg/m2(第1.2.4.6.8週目),ドキソルビシン40 mg/m2+エトポシド80 mg/m2(day 1-3,第1.3.5.7.9週目) | 9週間 |
引用文献
- 1)Fornasiero A, Daniele O, Ghiotto C, et al. Chemotherapy for invasive thymoma. A 13-year experience. Cancer. 1991; 68(1): 30-3. (IV)
- 2)Loehrer PJ Sr, Kim K, Aisner SC, et al. Cisplatin plus doxorubicin plus cyclophosphamide in metastatic or recurrent thymoma: final results of an intergroup trial. The Eastern Cooperative Oncology Group, Southwest Oncology Group, and Southeastern Cancer Study Group. J Clin Oncol. 1994; 12(6): 1164-8. (III)
- 3)Kunitoh H, Tamura T, Shibata T, et al; JCOG Lung Cancer Study Group. A phase-II trial of dose-dense chemotherapy in patients with disseminated thymoma: report of a Japan Clinical Oncology Group trial(JCOG 9605). Br J Cancer. 2009; 101(9): 1549-54. (III)
- 4)Kim ES, Putnam JB, Komaki R, et al. Phase II study of a multidisciplinary approach with induction chemotherapy, followed by surgical resection, radiation therapy, and consolidation chemotherapy for unresectable malignant thymomas: final report. Lung Cancer. 2004; 44(3): 369-79. (III)
- 5)Yokoi K, Matsuguma H, Nakahara R, et al. Multidisciplinary treatment for advanced invasive thymoma with cisplatin, doxorubicin, and methylprednisolone. J Thorac Oncol. 2007; 2(1): 73-8. (III)
- 6)Loehrer PJ Sr, Jiroutek M, Aisner S, et al. Combined etoposide, ifosfamide, and cisplatin in the treatment of patients with advanced thymoma and thymic carcinoma: an intergroup trial. Cancer. 2001; 91(11): 2010-5. (III)
- 7)Lemma GL, Lee JW, Aisner SC, et al. Phase II study of carboplatin and paclitaxel in advanced thymoma and thymic carcinoma. J Clin Oncol. 2011; 29(15): 2060-5. (III)
- 8)Giaccone G, Ardizzoni A, Kirkpatrick A, et al. Cisplatin and etoposide combination chemotherapy for locally advanced or metastatic thymoma. A phase II study of the European Organization for Research and Treatment of Cancer Lung Cancer Cooperative Group. J Clin Oncol. 1996; 14(3): 814-20. (III)
- 9)Bonomi PD, Finkelstein D, Aisner S, et al. EST 2582 phase II trial of cisplatin in metastatic or recurrent thymoma. Am J Clin Oncol. 1993; 16(4): 342-5. (III)
- 10)Liang Y, Padda SK, Riess JW, et al. Pemetrexed in patients with thymic malignancies previously treated with chemotherapy. Lung Cancer. 2015; 87(1): 34-8. (III)
- 11)Loehrer PJ Sr, Wang W, Johnson DH, et al; Eastern Cooperative Oncology Group Phase II Trial. Octreotide alone or with prednisone in patients with advanced thymoma and thymic carcinoma: an Eastern Cooperative Oncology Group Phase II Trial. J Clin Oncol. 2004; 22(2): 293-9. (III)
- 12)Palmieri G, Montella L, Martignetti A, Muto P, Di Vizio D, De Chiara A, Lastoria S. Somatostatin analogs and prednisone in advanced refractory thymic tumors. Cancer. 2002; 94(5): 1414-20. (IV)
- 13)Hirai F, Yamanaka T, Taguchi K, et al; West Japan Oncology Group. A multicenter phase II study of carboplatin and paclitaxel for advanced thymic carcinoma: WJOG4207L. Ann Oncol. 2015; 26(2): 363-8. (III)
- 14)Giaccone G, Rajan A, Ruijter R, et al. Imatinib mesylate in patients with WHO B3 thymomas and thymic carcinomas. J Thorac Oncol. 2009; 4(10): 1270-3. (III)
- 15)Thomas A, Rajan A, Berman A, et al. Sunitinib in patients with chemotherapy-refractory thymoma and thymic carcinoma: an open-label phase 2 trial. Lancet Oncol. 2015; 16(2): 177-86. (III)
- 16)Kossai M, Duchemann B, Boutros C, et al. Antitumor activity in advanced cancer patients with thymic malignancies enrolled in early clinical drug development programs(Phase I trials)at Gustave Roussy. Lung Cancer. 2015; 89(3): 306-10. (III)
- 17)Lopez-Chavez A, Thomas A, Rajan A, et al. Molecular profiling and targeted therapy for advanced thoracic malignancies: a biomarker-derived, multiarm, multihistology phase II basket trial. J Clin Oncol. 2015; 33(9): 1000-7. (III)
参考文献
- 1)Thomas A, Rajan A, Szabo E, et al. A phase I/II trial of belinostat in combination with cisplatin, doxorubicin, and cyclophosphamide in thymic epithelial tumors: a clinical and translational study. Clin Cancer Res. 2014; 20(21): 5392-402. (III)
- 2)Rajan A, Carter CA, Berman A, et al. Cixutumumab for patients with recurrent or refractory advanced thymic epithelial tumours: a multicentre, open-label, phase 2 trial. Lancet Oncol. 2014; 15(2): 191-200. (III)
- 3)Korst RJ, Bezjak A, Blackmon S, et al. Neoadjuvant chemoradiotherapy for locally advanced thymic tumors: a phase II, multi-institutional clinical trial. J Thorac Cardiovasc Surg. 2014; 147(1): 36-44. (III)
- 4)Wheler J, Hong D, Swisher SG, et al. Thymoma patients treated in a phase I clinic at MD Anderson Cancer Center: responses to mTOR inhibitors and molecular analyses. Oncotarget. 2013; 4(6): 890-8. (III)
- 5)Park S, Ahn MJ, Ahn JS, et al. A prospective phase II trial of induction chemotherapy with docetaxel/cisplatin for Masaoka stage III/IV thymic epithelial tumors. J Thorac Oncol. 2013; 8(7): 959-66. (III)
- 6)Palmieri G, Marino M, Buonerba C, et al. Imatinib mesylate in thymic epithelial malignancies. Cancer Chemother Pharmacol. 2012; 69(2): 309-15. (III)
- 7)Giaccone G, Rajan A, Berman A, et al. Phase II study of belinostat in patients with recurrent or refractory advanced thymic epithelial tumors. J Clin Oncol. 2011; 29(15): 2052-9. (III)
- 8)Kunitoh H, Tamura T, Shibata T, et al; JCOG Lung Cancer Study Group. A phase II trial of dose-dense chemotherapy, followed by surgical resection and/or thoracic radiotherapy, in locally advanced thymoma: report of a Japan Clinical Oncology Group trial(JCOG 9606). Br J Cancer. 2010; 103(1): 6-11. (III)
- 9)Grassin F, Paleiron N, André M, et al. Combined etoposide, ifosfamide, and cisplatin in the treatment of patients with advanced thymoma and thymic carcinoma. A French experience. J Thorac Oncol. 2010; 5(6): 893-7. (III)
- 10)Palmieri G, Merola G, Federico P, et al. Preliminary results of phase II study of capecitabine and gemcitabine(CAP-GEM)in patients with metastatic pretreated thymic epithelial tumors(TETs). Ann Oncol. 2010; 21(6): 1168-72. (III)
- 11)Wright CD, Choi NC, Wain JC, et al. Induction chemoradiotherapy followed by resection for locally advanced Masaoka stage III and IVA thymic tumors. Ann Thorac Surg. 2008; 85(2): 385-9. (III)
- 12)Chen YY, Huang CH, Tang Y, et al. Concurrent chemoradiotherapy for unresectable thymic carcinoma. Chang Gung Med J. 2004; 27(7): 515-22. (III)
- 13)Hanna N, Gharpure VS, Abonour R, et al. High-dose carboplatin with etoposide in patients with recurrent thymoma: the Indiana University experience. Bone Marrow Transplant. 2001; 28(5): 435-8. (IV)
- 14)Nakamura Y, Kunitoh H, Kubota K, et al. Platinum-based chemotherapy with or without thoracic radiation therapy in patients with unresectable thymic carcinoma. Jpn J Clin Oncol. 2000; 30(9): 385-8. (III)
- 15)Berruti A, Borasio P, Gerbino A, et al. Primary chemotherapy with adriamycin, cisplatin, vincristine and cyclophosphamide in locally advanced thymomas: a single institution experience. Br J Cancer. 1999; 81(5): 841-5. (III)
- 16)Loehrer PJ Sr, Chen M, Kim K, et al. Cisplatin, doxorubicin, and cyclophosphamide plus thoracic radiation therapy for limited-stage unresectable thymoma: an intergroup trial. J Clin Oncol. 1997; 15(9): 3093-9. (III)
- 17)Gordon MS, Battiato LA, Gonin R, et al. A phase II trial of subcutaneously administered recombinant human interleukin-2 in patients with relapsed/refractory thymoma. J Immunother Emphasis Tumor Immunol. 1995; 18(3): 179-84. (IV)
- 18)Oshita F, Kasai T, Kurata T, et al. Intensive chemotherapy with cisplatin, doxorubicin, cyclophosphamide, etoposide and granulocyte colony-stimulating factor for advanced thymoma or thymic cancer: preliminary results. Jpn J Clin Oncol. 1995; 25(5): 208-12. (III)
- 19)Palmieri G, Buonerba C, Ottaviano M, et al. Capecitabine plus gemcitabine in thymic epithelial tumors: final analysis of a Phase II trial. Future Oncol. 2014; 10(14): 2141-7. (III)
- 20)Inoue A, Sugawara S, Harada M, et al. Phase II study of Amrubicin combined with carboplatin for thymic carcinoma and invasive thymoma: North Japan Lung Cancer group study 0803. J Thorac Oncol. 2014; 9(12): 1805-9. (III)