2
Ⅲ.小細胞肺癌
進展型小細胞肺癌の1次治療
文献検索と採択

本文中に用いた略語および用語の解説
| AMR | アムルビシン | ETP | エトポシド |
|---|---|---|---|
| CBDCA | カルボプラチン | GEM | ゲムシタビン |
| CDDP | シスプラチン | PTX | パクリタキセル |
| CPA | シクロフォスファミド | VCR | ビンクリスチン |
| CPT-11 | イリノテカン | VNR | ビノレルビン |
| DTX | ドセタキセル | プラチナ製剤 | CDDPとCBDCAの総称 |
| DXR | ドキソルビシン | ||
| ACE | ドキソルビシン+シクロフォスファミド+エトポシド | ||
| CAV | シクロフォスファミド+ドキソルビシン+ビンクリスチン | ||
| CE | カルボプラチン+エトポシド | ||
| PA | シスプラチン+アムルビシン | ||
| PE | シスプラチン+エトポシド | ||
| PI | シスプラチン+イリノテカン | ||
| SPE | 分割投与シスプラチン+エトポシド | ||
| ECOG | Eastern Cooperative Oncology Group | 米国東海岸癌臨床試験グループ | |
| JCOG | Japan Clinical Oncology Group | 日本臨床腫瘍研究グループ | |
| PCI | prophylactic cranial irradiation | 予防的全脳照射 | |
| PS | performance status | 一般状態 | |
| SCLC | small cell lung cancer | 小細胞肺癌 | |
樹形図
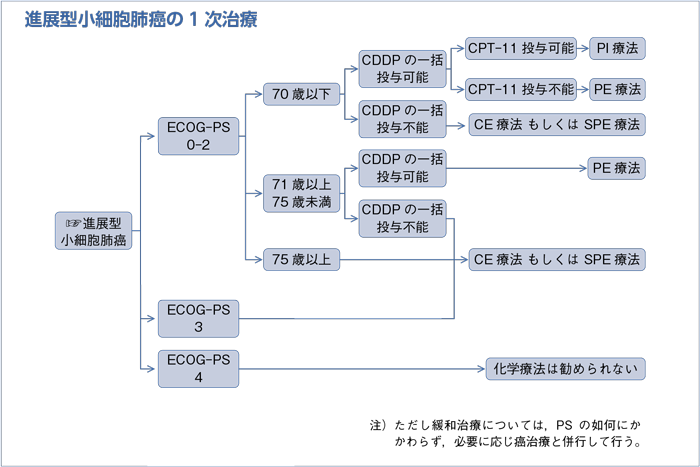
2-1.進展型小細胞肺癌の1次治療
- 推 奨
a.PS 0-3の進展型小細胞肺癌に対する化学療法は,プラチナ製剤を含む併用化学療法を行うよう勧められる。
- a-1.70歳以下のPS 0-2の患者にはシスプラチン+イリノテカンが推奨される。(グレードA)
- a-2.71歳以上75歳未満のPS 0-2患者および70歳以下でイリノテカンの毒性が懸念される患者にはシスプラチン+エトポシドが推奨される。(グレードA)
- a-3.下記の患者にはシスプラチン分割もしくはカルボプラチン+エトポシドが推奨される。(グレードB)
- PS 0-2でシスプラチンの一括投与ができない
- 75歳以上
- PS 3
b.進展型小細胞肺癌に対する初回治療は4コース行うよう勧められる。(グレードA)
c.維持療法の有用性は認められておらず,行わないよう勧められる。(グレードD)
d.大量化学療法あるいは単位時間あたりの投与量を増やし,治療強度を高めた化学療法は行わないよう勧められる。(グレードD)
e.化学療法後のPCIは行わないよう勧められる。(グレードD)
エビデンス
- a.
- 1960年代,進展型小細胞肺癌患者を対象に行われたシクロフォスファミド(CPA)単剤と緩和治療(BSC;best supportive care)との比較試験で,化学療法群の生存期間が約2倍に延長することが示された1)。1970年代にはCPA単剤と多剤併用化学療法との比較試験が行われ,多剤併用化学療法での生存期間延長が示された2)~4)。1970~80年代はCPAを含む併用化学療法が広く用いられていたが,1980年代以降CDDP+ETP(PE)との比較試験が行われた。PEとDXR+CPA+ETP(ACE)との比較試験では,奏効率,生存期間に有意差はなく,ACEが有意に好中球減少,敗血症の割合が高かったことが示されている5)。2000年に報告されたCCDPを含む化学療法とそれ以外との比較試験のメタアナリシスでは,CDDPを含むレジメンが奏効率および1年生存率が有意に高く,治療関連死には差を認めなかったとしている6)。以上より,2000年以降世界的にはPEが標準治療と考えられてきた。
また,日本で70歳以上かつPS 0-2の患者を対象にAMR単剤とCBDCA+ETP(CE)との比較試験が行われたが,AMR単剤群で治療関連死が多く認められ,試験は早期中止となった。したがって70歳以上においても,AMR単剤療法は推奨されず,プラチナ併用化学療法が推奨される7)。 - a-1.
- 本邦で行われた70歳以下のPS 0-2を対象とした,PEとCDDP+CTP-11(PI)との比較試験(JCOG9511)の結果,PIが有意に生存期間を延長することが示された(生存期間中央値9.4カ月vs 12.8カ月)8)。その後,北米を中心にPEとPIとの比較試験の追試が行われたが,JCOG9511の結果を再現することはできなかった9)~11)。しかし,プラチナ製剤+ETPとプラチナ製剤+CPT-11とのランダム化試験のメタアナリシスでは,CPT-11群が有意に奏効率が高く,生存期間を延長し,血液毒性が軽度で,嘔吐,下痢の頻度が高いことが示されている12)~14)。また,PIとCDDP+AMR(PA)との比較試験が本邦で行われ,PAはPIに対する非劣性を証明することはできなかった(生存期間中央値15.0カ月vs 18.3カ月)15)。これらの結果から,JCOG9511の対象となったPS 0-2の70歳以下の患者にはPIが推奨される。
- a-2.
- 1980年代以降PEは小細胞肺癌の治療に頻用され,海外の第Ⅲ相試験では年齢制限なく臨床試験が行われていることが多い。日本では75歳未満のPS 0-3の小細胞肺癌(限局型,進展型を含む)に対しPEとCPA+DXR+VCR(CAV)とCAV/PE交代療法を比較する第Ⅲ相試験が行われ,PE療法とCAV/PE療法の奏効率がCAVより有意に高く,毒性は許容範囲であった16)。PIに関して,71歳以上の高齢者の小細胞肺癌に対する本邦のエビデンスは現時点では存在しない。しかしながら,非小細胞肺癌に対する治療としてもCDDP+CPT-11は使用されており,日本において74歳までのPS 0-1の進行期非小細胞肺癌を対象にCDDP+CPT-11,CDDP+GEM,CDDP+VCR,CBDCA+DTXの4群を比較する第Ⅲ相試験17)の結果より毒性は許容範囲であることから,実地臨床では74歳までの小細胞肺癌に使用されることもある。また,1つの第Ⅲ相試験のサブセット解析のみであるが,CDDPを含む併用化学療法のランダム化試験に参加した70歳以上の高齢者の解析では,若年者との比較で明らかな差は認めていないとの報告もある18)。CPT-11は下痢が臨床的に問題であり,また間質性肺炎を有する患者には禁忌とされている。そのため,下痢の発症が懸念される患者にはPEが推奨され,間質性肺炎の発症が懸念される患者にはPEが選択肢になる。
- a-3.
- JCOGは,70歳以上かつPS 0-2の高齢者および70歳以下のPS 3の患者を対象にsplit PE(SPE:CDDP 3日間分割投与)とCBDCA+ETP(CE)との比較試験を行い,CE群で血小板減少が多く,奏効率,生存期間はほぼ同様であった(JCOG9702)19)。本邦で行われたPS 3に対する治療効果に関するエビデンスはJCOG9702のサブセット解析のみである。CDDPの毒性が懸念される患者に対しては,CBDCAを用いることも推奨される。また,海外の試験でも,約15%のPS 3を含めた第Ⅲ相試験20)もあり,いずれもサブセット解析のみではあるが,PS 3に関しては小細胞肺癌に対する治療効果によってPSの改善が得られる可能性があれば化学療法の対象になり得る。PS 4を含めた第Ⅲ相試験21)もあるが,PS 4の登録は3%とごくわずかである。PS 4を主たる対象にしての前向き試験の評価は行われておらず,進展型小細胞癌に関するエビデンスはないのが現状である。
- b.
- 治療期間に関し,PI,PEを用いた臨床試験の多くは投与コース数を4コースとしていることより投与コース数は4コースが推奨される。a-3で述べたPE(3日間分割投与)とCBDCA+ETP(CE)との比較試験(JCOG9702)においても投与コース数は4コースとされている。
- c.
- 維持療法に関しては,メタアナリシスで無増悪生存期間の延長が示されたが,1年生存率や生存期間の延長については明らかな有用性は示されておらず,行わないよう勧められる22)。
- d.
- 大量化学療法あるいは治療強度を高めた治療法に関しては,最近の報告でも有用性を示したものはなく,一般診療では行わないよう勧められる23)~27)。
- e.
- 詳細な解説については,予防的全脳照射(PCI)の項を参照。
引用文献
- 1)Green RA, Humphrey E, Close H, et al. Alkylating agents in bronchogenic carcinoma. Am J Med. 1969; 46(4): 516-25. (II)
- 2)Edmonson JH, Lagakos SW, Selawry OS, et al. Cyclophosphamide and CCNU in the treatment of inoperable small cell carcinoma and adenocarcinoma of the lung. Cancer Treat Rep. 1976; 60(7): 925-32. (II)
- 3)Alberto P, Brunner KW, Martz G, et al. Treatment of bronchogenic carcinoma with simultaneous or sequential combination chemotherapy, including methotrexate, cyclophosphamide, procarbazine and vincristine. Cancer. 1976; 38(6): 2208-16. (II)
- 4)Lowenbraun S, Bartolucci A, Smalley RV, et al. The superiority of combination chemotherapy over single agent chemotherapy in small cell lung carcinoma. Cancer. 1979; 44(2): 406-13. (II)
- 5)Baka S, Califano R, Ferraldeschi R, et al. Phase III randomised trial of doxorubicin-based chemotherapy compared with platinum-based chemotherapy in small-cell lung cancer. Br J Cancer. 2008; 99(3): 442-7. (II)
- 6)Pujol JL, Carestia L, Daurès JP. Is there a case for cisplatin in the treatment of small-cell lung cancer? A meta-analysis of randomized trials of a cisplatin-containing regimen versus a regimen without this alkylating agent. Br J Cancer. 2000; 83(1): 8-15. (I)
- 7)Sekine I, Okamoto H, Horai T, et al. A randomized phase III study of single-agent amrubicin vs. carboplatin/etoposide in elderly patients with extensive-disease small-cell lung cancer. Clin Lung Cancer 2014; 15(2): 96-102. (II)
- 8)Noda K, Nishiwaki Y, Kawahara M, et al. Irinotecan plus cisplatin compared with etoposide plus cisplatin for extensive small-cell lung cancer. N Engl J Med. 2002; 346(2): 85-91. (II)
- 9)Hanna N, Bunn PA Jr, Langer C, et al. Randomized phase III trial comparing irinotecan/cisplatin with etoposide/cisplatin in patients with previously untreated extensive-stage disease small-cell lung cancer. J Clin Oncol. 2006; 24(13): 2038-43. (II)
- 10)Lara PN Jr, Natale R, Crowley J, et al. Phase III trial of irinotecan/cisplatin compared with etoposide/cisplatin in extensive-stage small-cell lung cancer: clinical and pharmacogenomic results from SWOG S0124. J Clin Oncol. 2009; 27(15): 2530-5. (II)
- 11)Zatloukal P, Cardenal F, Szczesna A, et al. A multicenter international randomized phase III study comparing cisplatin in combination with irinotecan or etoposide in previously untreated small-cell lung cancer patients with extensive disease. Ann Oncol. 2010; 21(9): 1810-6. (II)
- 12)Jiang L, Yang KH, Mi DH, et al. Safety of irinotecan/cisplatin versus etoposide/cisplatin for patients with extensive-stage small-cell lung cancer: a metaanalysis. Clin Lung Cancer. 2007; 8(8): 497-501. (I)
- 13)Jiang J, Liang X, Zhou X, et al. A meta-analysis of randomized controlled trials comparing irinotecan/platinum with etoposide/platinum in patients with previously untreated extensive-stage small cell lung cancer. J Thorac Oncol. 2010; 5(6): 867-73. (I)
- 14)Lima JP, dos Santos LV, Sasse EC, et al. Camptothecins compared with etoposide in combination with platinum analog in extensive stage small cell lung cancer: systematic review with meta-analysis. J Thorac Oncol. 2010; 5(12): 1986-93. (I)
- 15)Satouchi M, Kotani Y, Shibata T, et al. Phase III study comparing amrubicin plus cisplatin with irinotecan plus cisplatin in the treatment of extensive-disease small-cell lung cancer: JCOG 0509. J Clin Oncol. 2014; 32(12): 1262-8. (II)
- 16)Fukuoka M, Furuse K, Saijo N, et al. Randomized trial of cyclophosphamide, doxorubicin, and vincristine versus cisplatin and etoposide versus alternation of these regimens in small-cell lung cancer. J Natl Cancer Inst. 1991; 83(12): 855-61. (II)
- 17)Ohe Y, Ohashi Y, Kubota K, et al. Randomized phase III study of cisplatin plus irinotecan versus carboplatin plus paclitaxel, cisplatin plus gemcitabine, and cisplatin plus vinorelbine for advanced non-small-cell lung cancer: Four-Arm Cooperative Study in Japan. Ann Oncol. 2007; 18(2): 317-23. (II)
- 18)Safont MJ, Artal-Cortes A, Sirera R, et al. Retrospective study of efficacy and toxicity on patients older than 70 years within a randomized clinical trial of two cisplatin-based combinations in patients with small-cell lung cancer. Lung Cancer. 2009; 63(1): 83-7. (III)
- 19)Okamoto H, Watanabe K, Kunikane H, et al. Randomised phase III trial of carboplatin plus etoposide vs split doses of cisplatin plus etoposide in elderly or poor-risk patients with extensive disease small-cell lung cancer: JCOG 9702. Br J Cancer. 2007; 97(2): 162-9. (II)
- 20)Souhami RL, Spiro SG, Rudd RM, et al. Five-day oral etoposide treatment for advanced small-cell lung cancer: randomized comparison with intravenous chemotherapy. J Natl Cancer Inst. 1997; 89(8): 577-80. (II)
- 21)Girling DJ. Comparison of oral etoposide and standard intravenous multidrug chemotherapy for small-cell lung cancer: a stopped multicentre randomised trial. Medical Research Council Lung Cancer Working Party. Lancet. 1996; 348(9027): 563-6. (II)
- 22)Zhou H, Zeng C, Wei Y, et al. Duration of chemotherapy for small cell lung cancer: a meta-analysis. PLoS One. 2013; 8(8): e73805. (I)
- 23)Lorigan P, Woll PJ, O’Brien ME, et al. Randomized phase III trial of dose-dense chemotherapy supported by whole-blood hematopoietic progenitors in better-prognosis small-cell lung cancer. J Natl Cancer Inst. 2005; 97(9): 666-74. (II)
- 24)Buchholz E, Manegold C, Pilz L, et al. Standard versus dose-intensified chemotherapy with sequential reinfusion of hematopoietic progenitor cells in small cell lung cancer patients with favorable prognosis. J Thorac Oncol. 2007; 2(1): 51-8. (II)
- 25)Leyvraz S, Pampallona S, Martinelli G, et al; Solid Tumors Working Party of the European Group for Blood and Marrow Transplantation. A threefold dose intensity treatment with ifosfamide, carboplatin, and etoposide for patients with small cell lung cancer: a randomized trial. J Natl Cancer Inst. 2008; 100(8): 533-41. (II)
- 26)Heigener DF, Manegold C, Jäger E, et al. Multicenter randomized open-label phase III study comparing efficacy, safety, and tolerability of conventional carboplatin plus etoposide versus dose-intensified carboplatin plus etoposide plus lenograstim in small-cell lung cancer in“extensive disease”stage. Am J Clin Oncol. 2009; 32(1): 61-4. (II)
- 27)Jiang J, Shi HZ, Deng JM, et al. Efficacy of intensified chemotherapy with hematopoietic progenitors in small-cell lung cancer: A meta-analysis of the published literature. Lung Cancer. 2009; 65(2): 214-8. (I)
レジメン:進展型小細胞肺癌
| PI療法 | CDDP | 60 mg/m2,day 1 | q4w |
|---|---|---|---|
| CPT-11 | 60 mg/m2,day 1,8,15 | ||
| PE療法 | CDDP | 80 mg/m2,day 1 | q3w |
| ETP | 100 mg/m2,day 1,2,3 | ||
| CE療法 | CBDCA | AUC=5,day 1 | q3~4 w |
| ETP | 80 mg/m2,day 1,2,3 | ||
| SPE(CDDP分割)療法 | CDDP | 25 mg/m2,day 1,2,3 | q3~4 w |
| ETP | 80 mg/m2,day 1,2,3 |