2
Ⅱ.治 療
集学的治療
2-1.集学的治療における化学療法
文献検索と採択
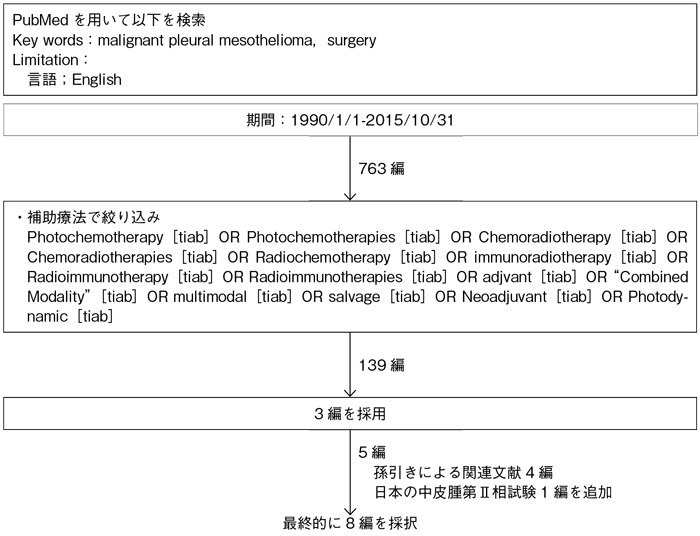
2-1.集学的治療における化学療法
- 推 奨
- 術前・術後の化学療法を行うことを考慮してもよい。(グレードC1)
エビデンス
医学的に手術可能なⅠ-Ⅲ期の悪性胸膜中皮腫症例には,術前または術後のどちらかに集学的治療の一環として化学療法を施行することができる。Sugarbakerらの報告以来,手術(胸膜肺全摘術),全身化学療法,片側胸郭照射を併用する三者併用療法(trimodality therapy),または,手術(胸膜切除・肺剥皮術)と全身化学療法の二者併用療法(Bimodality therapy)の一環として施行されてきた1)2)。術前化学療法,手術,術後片側胸郭照射による三者併用療法の安全性および忍容性については一定の評価が得られているが3)~7),周術期化学療法を術前または術後のどちらに行うべきかの前向き比較試験の報告はない。
現時点での多剤併用レジメンのゴールドスタンダートはCDDP/PEMであり3)~5),他にCDDP/GEM6),CBDCA/GEM7)などの報告もある。CDDP/PEMによる術前化学療法を用いた三者併用療法を完遂した患者の生存期間中央値は29.1カ月,2年生存率は61.2%と報告されており,化学療法に対する良好な反応がその後の手術適応決定を左右する因子となる可能性が指摘されている3)。
三者併用療法の付加的療法として術中胸腔内温熱化学療法が有効との報告もある8)。
現時点での多剤併用レジメンのゴールドスタンダートはCDDP/PEMであり3)~5),他にCDDP/GEM6),CBDCA/GEM7)などの報告もある。CDDP/PEMによる術前化学療法を用いた三者併用療法を完遂した患者の生存期間中央値は29.1カ月,2年生存率は61.2%と報告されており,化学療法に対する良好な反応がその後の手術適応決定を左右する因子となる可能性が指摘されている3)。
三者併用療法の付加的療法として術中胸腔内温熱化学療法が有効との報告もある8)。
引用論文
- 1)Sugarbaker DJ, Flores RM, Jaklitsch MT, et al. Resection margins, extrapleural nodal status, and cell type determine postoperative long-term survival in trimodality therapy of malignant pleural mesothelioma: results in 183 patients. J Thorac Cardiovasc Surg. 1999; 117(1): 54-63; discussion 63-5. (IV)
- 2)Bölükbas S, Manegold C, Eberlein M, et al. Survival after trimodality therapy for malignant pleural mesothelioma: Radical Pleurectomy, chemotherapy with Cisplatin/Pemetrexed and radiotherapy. Lung Cancer. 2011; 71(1): 75-81. (IV)
- 3)Krug LM, Pass HI, Rusch VW, et al. Multicenter phaseⅡ trial of neoadjuvant pemetrexed plus cisplatin followed by extrapleural pneumonectomy and radiation for malignant pleural mesothelioma. J Clin Oncol. 2009; 27(18): 3007-13. (IV)
- 4)Van Schil PE, Baas P, Gaafar R, et al; European Organisation for Research and Treatment of Cancer(EORTC)Lung Cancer Group. Trimodality therapy for malignant pleural mesothelioma: results from an EORTC phaseⅡ multicentre trial. Eur Respir J. 2010; 36(6): 1362-9. (IV)
- 5)Hasegawa S, Okada M, Tanaka F, et al. Trimodality strategy for treating malignant pleural mesothelioma: results of a feasibility study of induction pemetrexed plus cisplatin followed by extrapleural pneumonectomy and postoperative hemithoracic radiation(Japan Mesothelioma Interest Group 0601 Trial). Int J Clin Oncol. 2016; 21(3): 523-30. (IV)
- 6)Weder W, Stahel RA, Bernhard J, et al; Swiss Group for Clinical Cancer Research. Multicenter trial of neo-adjuvant chemotherapy followed by extrapleural pneumonectomy in malignant pleural mesothelioma. Ann Oncol. 2007; 18(7): 1196-202. (IV)
- 7)Rea F, Marulli G, Bortolotti L, et al. Induction chemotherapy, extrapleural pneumonectomy(EPP)and adjuvant hemi-thoracic radiation in malignant pleural mesothelioma(MPM): Feasibility and results. Lung Cancer. 2007; 57(1): 89-95. (IV)
- 8)Sugarbaker DJ, Gill RR, Yeap BY, et al. Hyperthermic intraoperative pleural cisplatin chemotherapy extends interval to recurrence and survival among low-risk patients with malignant pleural mesothelioma undergoing surgical macroscopic complete resection. J Thorac Cardiovasc Surg. 2013; 145(4): 955-63. (IV)
2-2.集学的治療における放射線治療
文献検索と採択
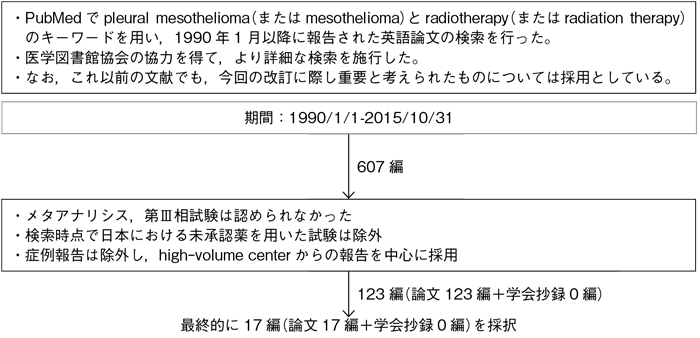
2-2.集学的治療における放射線治療
- 推 奨
a.胸膜肺全摘術(EPP)が施行された症例に対する片側胸郭照射は,PSが良好な症例に行うことを考慮してよい。(グレードC1)
b.胸膜切除・肺剥皮術(P/D)後の症例に対する片側胸郭照射を行うよう勧めるだけの根拠はない。(グレードC2)
c.放射線治療の方法として,3次元原体放射線治療(3D-CRT)または,強度変調放射線治療(IMRT)を行うことを考慮してもよい。(グレードC1)
エビデンス
- a.
- 放射線治療は集学的治療の一つとして,EPP後の片側胸郭照射として用いられてきた。Memorial Sloan-Kettering Cancer Center(MSKCC)のグループは通常照射による54 Gyの片側胸郭へのEPP後の照射を行っており,1993~95年に行った55例の報告では,局所領域再発を13%に認め,4%は局所領域再発のみであった1)。一方,低線量(30.6 Gy)での片側胸郭照射を行ったHarvard大学のグループからの46例の報告では,局所領域再発を50%に認め,13%が局所領域再発のみであったとしている2)3)。以上から,線量増加による局所領域制御の改善の可能性は考えられる。しかし,同じくMSKCCのグループは,同様の方法で症例を重ね,1993~2008年に行われた78例の解析において,局所領域制御が約40%に上ったと報告している(局所領域再発:41%,局所領域再発のみ:19%)4)。
悪性胸膜中皮腫に対する治療成績の改善のため,上記のような片側胸郭照射は必要であるとされながらも,いずれの報告も単施設からのretrospective dataもしくは第Ⅱ相試験であり,片側胸郭照射の可否を目的とした第Ⅲ相試験は現在のところ存在しないため,推奨グレードC1とした。 - b.
- MSKCCのグループは,1974~2003年にかけてP/Dを施行後,通常照射での片側胸郭照射(median 42.5 Gy)を123症例に行い,2年全生存率23%,1年局所制御割合42%であった。有害事象はGrade 3以上放射線肺臓炎が13例(10.6%),うち1例がGrade 5であったと報告している。この結果からP/D後の片側胸郭照射は有効な治療選択肢ではないと結論付けている5)。一方,近年,P/D後にIMRTを施行した結果が同グループから報告されている。EPP以外の非切除例およびP/D施行後,IMRTを用いた片側胸郭照射を行った36症例において,P/D例および非手術例の2年生存率がそれぞれ53%,28%であった一方で,Grade 3以上の放射線肺臓炎を7例(20%)に認め,うち1例がGrade 5であり実行可能と報告しているが,重篤な放射線肺臓炎の頻度は依然として高い6)。MD Anderson Cancer Center(MDACC)のグループは,P/D施行後,IMRTにて45 Gyの片側胸郭照射を行った24症例(P/D-IMRT群)において,同時期にEPP施行後にIMRTを行った24例(EPP-IMRT群)とのマッチングによる比較を行っており,P/D-IMRT群とEPP-IMRT群において,生存期間中央値は28.4カ月と14.2カ月(P=0.04)でP/D-IMRT群でやや良好であったが,Grade 4-5の有害事象に有意差は認めなかった(0% vs 12.5%,P=0.23)と報告している7)。
いずれにしてもP/D施行後のIMRTも含めた片側胸郭照射は有害事象の割合が多いと考えられ,これを行うだけの根拠はない。米国のNational Comprehensive Cancer Network(NCCN)8)および欧州のEuropean Respiratory Society(ERS)/European Society of Thoracic Surgeons(ESTS)からのガイドライン9)においても,肺が残存する状況でのIMRTも含めた片側胸郭照射は毒性の観点からも行うことは推奨していない。したがって,P/D後の症例に対する片側胸郭照射を行うよう勧められるだけの科学的根拠は明確でなく,推奨グレードをC2とした。 - c.
- EPP後の片側胸郭照射の方法として3D-CRTが推奨される10)。しかし,近年のコンピュータ技術による最適化計算により,照射装置から放射線が出る部分の形状を特殊な方法で段階的に変化させながら照射する強度変調放射線治療(intensity-modulated radiotherapy:IMRT)が可能となった。EPP後の標的体積は胸腔から腹腔を含む広範囲かつ複雑な形状を呈しており,IMRTは3D-CRTよりも標的体積への線量分布の改善が期待できる11)。
EPP後にIMRTを用いた治療成績として,63例において照射野内再発が僅か5%と良好な成績が報告されている12)。さらに3D-CRTを施行した24例とIMRTを施行した14例の比較では,IMRT群で有意に局所再発が低かったとの報告がある(41.7% vs 14.3%,P=0.03)13)。IMRTに関するレビューでもIMRTを施行することで従来の成績を超える可能性はあるとしている14)15)。しかし,いずれの報告も単施設からのretrospective dataであり,IMRTと3D-CRTを比較した第Ⅲ相試験は現在のところ存在しないことから,放射線治療の方法として3D-CRTまたはIMRTを行うことを考慮してもよく,推奨グレードをC1とした。
ただし,EPP後のIMRTによる有害事象として,特に放射線肺臓炎に留意する必要がある。Harvard大学からの初期報告では,13例中6例に致死的な放射線肺臓炎を生じ,対側健常肺への照射線量が問題とされた16)。5 Gyおよび20 Gy以上照射された体積(V5%,V20%),平均線量(MLD)の中央値はそれぞれ92.4%,15.7%,13.8 Gyであり,特に低線量域の拡大を示すパラメータを抑制することが重要であることが示された。IMRTを施行した63例の報告では6例(9.5%)の呼吸器関連死を認めており,呼吸器関連死群の肺V20%中央値は9.8%であったのに対し,呼吸器関連死を認めなかった群では3.6%であり,多変量解析にて有意な因子であったとしている17)。以上の報告から,IMRTによる放射線肺臓炎は対側健常肺への照射線量に依存する傾向にあり,MDACCのグループからは厳格な線量制約(V5%<60%,V20%<20%,MLD<8.5 Gy)を守ることで肺毒性を低減できる可能性を示唆している14)。
このようにEPP後のIMRTは局所制御やリスク臓器保護の面で期待されるものの,重篤な放射線肺臓炎などの有害事象を引き起こす可能性のある方法であるため,適切な線量制約を設定したうえで治療計画に熟練する必要がある。前述のERS/ESTSのガイドラインでは,「specialized center only」で行うことが推奨されており9),EPP後のIMRTは症例数が見込める経験のある施設またはプロトコールを確立したうえで行うべきである。
引用論文
- 1)Rusch VW, Rosenzweig K, Venkatraman E, et al. A phaseⅡ trial of surgical resection and adjuvant high-dose hemithoracic radiation for malignant pleural mesothelioma. J Thorac Cardiovasc Surg. 2001; 122(4): 788-95. (IV)
- 2)Baldini EH. External beam radiation therapy for the treatment of pleural mesothelioma. Thorac Surg Clin. 2004; 14(4): 543-8. (VI)
- 3)Jänne PA, Baldini EH. Patterns of failure following surgical resection for malignant pleural mesothelioma. Thorac Surg Clin. 2004; 14(4): 567-73. (VI)
- 4)Gupta V, Krug LM, Laser B, et al. Patterns of local and nodal failure in malignant pleural mesothelioma after extrapleural pneumonectomy and photon-electron radiotherapy. J Thorac Oncol. 2009; 4(6): 746-50. (IV)
- 5)Gupta V, Mychalczak B, Krug L, et al. Hemithoracic radiation therapy after pleurectomy/decortication for malignant pleural mesothelioma. Int J Radiat Oncol Biol Phys. 2005; 63(4): 1045-52. (IV)
- 6)Rosenzweig KE, Zauderer MG, Laser B, et al. Pleural intensity-modulated radiotherapy for malignant pleural mesothelioma. Int J Radiat Oncol Biol Phys. 2012; 83(4): 1278-83. (IV)
- 7)Chance WW, Rice DC, Allen PK, et al. Hemithoracic intensity modulated radiation therapy after pleurectomy/decortication for malignant pleural mesothelioma: toxicity, patterns of failure, and a matched survival analysis. Int J Radiat Oncol Biol Phys. 2015; 91(1): 149-56. (IV)
- 8)National Comprehensive Cancer Network. NCCN Clinical Practice Guldlines. Malignant Pleural Mesothelioma. Ver. 2. 2015. (VI)
- 9)Scherpereel A, Astoul P, Baas P, et al; European Respiratory Society/European Society of Thoracic Surgeons Task Force. Guidelines of the European Respiratory Society and the European Society of Thoracic Surgeons for the management of malignant pleural mesothelioma. Eur Respir J. 2010; 35(3): 479-95. (VI)
- 10)Yajnik S, Rosenzweig KE, Mychalczak B, et al. Hemithoracic radiation after extrapleural pneumonectomy for malignant pleural mesothelioma. Int J Radiat Oncol Biol Phys. 2003; 56(5): 1319-26. (IV)
- 11)Krayenbuehl J, Oertel S, Davis JB, et al. Combined photon and electron three-dimensional conformal versus intensity-modulated radiotherapy with integrated boost for adjuvant treatment of malignant pleural mesothelioma after pleuropneumonectomy. Int J Radiat Oncol Biol Phys. 2007; 69(5): 1593-9. (IV)
- 12)Rice DC, Stevens CW, Correa AM, et al. Outcomes after extrapleural pneumonectomy and intensity-modulated radiation therapy for malignant pleural mesothelioma. Ann Thorac Surg. 2007; 84(5): 1685-92; discussion 1692-3. (IV)
- 13)Buduhan G, Menon S, Aye R, et al. Trimodality therapy for malignant pleural mesothelioma. Ann Thorac Surg. 2009; 88(3): 870-5; discussion 876. (IV)
- 14)Chi A, Liao Z, Nguyen NP, et al. Intensity-modulated radiotherapy after extrapleural pneumonectomy in the combined-modality treatment of malignant pleural mesothelioma. J Thorac Oncol. 2011; 6(6): 1132-41. (VI)
- 15)Rosenzweig KE. Current readings: improvements in intensity-modulated radiation therapy for malignant pleural mesothelioma. Semin Thorac Cardiovasc Surg. 2013; 25(3): 245-50. (VI)
- 16)Allen AM, Czerminska M, Jänne PA, et al. Fatal pneumonitis associated with intensity-modulated radiation therapy for mesothelioma. Int J Radiat Oncol Biol Phys. 2006; 65(3): 640-5. (IV)
- 17)Rice DC, Smythe WR, Liao Z, et al. Dose-dependent pulmonary toxicity after postoperative intensity-modulated radiotherapy for malignant pleural mesothelioma. Int J Radiat Oncol Biol Phys. 2007; 69(2): 350-7. (IV)